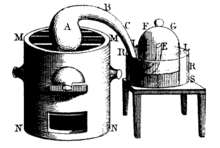
První experimenty
Jeden z prvních známých pokusů o tom, jak spalování potřebuje vzduch, provedl Řek Filón Byzantský ve 2. století před naším letopočtem. Ve svém díle Pneumatica napsal, že otočení nádoby dnem vzhůru nad hořící svíčkou a její oblití vodou znamená, že se do nádoby dostane trochu vody. Filón se domníval, že je to proto, že se vzduch proměnil v klasický živel oheň. To byl omyl. Dlouho poté Leonardo da Vinci správně přišel na to, že při hoření se spotřebovává vzduch, který vytlačuje vodu do nádoby.
Na konci 17. století Robert Boyle zjistil, že ke spalování je zapotřebí vzduch. Anglický chemik John Mayow k tomu dodal, že oheň potřebuje pouze část vzduchu. Tu nyní nazýváme kyslík (ve formě dioxygenu). Při jednom ze svých pokusů zjistil, že při vložení svíčky do uzavřené nádoby voda stoupá tak, aby nahradila čtvrtinu objemu vzduchu v nádobě, a teprve poté zhasne. Totéž se stalo, když do krabice vložil myš. Z toho vyvodil, že kyslík se používá k dýchání a hoření.
Teorie flogistonu
Robert Hooke, Ole Borch, Michail Lomonosov a Pierre Bayen prováděli v 17. a 18. století pokusy s kyslíkem. Nikdo z nich si nemyslel, že jde o chemický prvek. Důvodem byla pravděpodobně myšlenka flogistonové teorie. Ten podle většiny lidí způsoboval hoření a korozi.
J. J. Becher s ní přišel v roce 1667 a Georg Ernst Stahl ji doplnil v roce 1731. Flogistonová teorie tvrdila, že všechny hořlaviny se skládají ze dvou částí. Jedna část, nazývaná flogiston, se uvolňuje při hoření látky, která ho obsahuje.
Velmi hořlavé materiály, které zanechávají jen malé množství zbytků, jako je dřevo nebo uhlí, byly považovány za flogiston. Věci, které podléhají korozi, jako je železo, byly považovány za látky, které obsahují jen malé množství floglozidu. Vzduch nebyl součástí této teorie.
Discovery
Polský alchymista, filozof a lékař Michael Sendivogius hovořil o látce obsažené ve vzduchu a nazval ji "potravou života"., a touto látkou je kyslík. Sendivogius v letech 1598-1604 zjistil, že jde o stejnou látku, jaká vzniká při tepelném rozkladu dusičnanu draselného. Někteří lidé se domnívají, že to byl objev kyslíku, zatímco jiní s tím nesouhlasí.
Často se také uvádí, že kyslík poprvé objevil švédský lékárník Carl Wilhelm Scheele. Ten v roce 1771 vyrobil kyslík zahřátím oxidu rtuťnatého a některých dusičnanů. Scheele nazval plyn, který vyrobil, "ohnivý vzduch", protože to byl jediný známý plyn, který umožňoval hoření. Svůj objev zveřejnil v roce 1777.
1. srpna 1774 provedl britský duchovní Joseph Priestley pokus, při němž se sluneční světlo zaměřilo na oxid rtuťnatý ve skleněné trubici. Vznikl tak plyn, který nazval "deflogistický vzduch". Zjistil také, že svíčky v tomto plynu hoří jasněji a myši při jeho dýchání žijí déle. Když se plynu nadýchal, řekl (zjednodušeně řečeno): "Bylo to jako normální vzduch, ale moje plíce se poté cítily lehčí a snadnější." Své poznatky zveřejnil v roce 1775. Protože jeho poznatky byly publikovány jako první, bývá označován za objevitele kyslíku.
Francouzský chemik Antoine Lavoisier později prohlásil, že tuto látku také objevil. Priestly ho v roce 1774 navštívil a vyprávěl mu o svém pokusu. V témže roce Scheele také poslal Lavoisierovi dopis, v němž hovořil o svém objevu.
Lavoisierův příspěvek
Lavoisier provedl první hlavní pokusy s oxidací a poprvé správně vysvětlil, jak funguje spalování. Těmito a dalšími pokusy dokázal, že flogistonová teorie je chybná. Snažil se také dokázat, že látka objevená Priestleym a Scheelem je chemický prvek.
Při jednom pokusu Lavoisier zjistil, že při zahřívání cínu a vzduchu v uzavřené nádobě nedochází k nárůstu hmotnosti. Zjistil také, že po otevření nádoby se dovnitř dostává vzduch. Poté zjistil, že hmotnost cínu vzrostla o stejné množství, o jaké se zvětšil vniklý vzduch. Své poznatky zveřejnil v roce 1777. Napsal, že vzduch se skládá ze dvou plynů. Jeden nazval "životně důležitý vzduch" (kyslík), který je potřebný pro spalování a dýchání. Druhý nazval "azote" (dusík), což v řečtině znamená "neživý". Takto se dusík dodnes nazývá v některých jazycích, včetně francouzštiny.
Lavoisier přejmenoval "vitální vzduch" na "oxygène", což v řečtině znamená "výrobce z kyselin". Nazval ho tak proto, že se domníval, že kyslík je obsažen ve všech kyselinách, což bylo nesprávné. Mnoho chemiků si uvědomilo, že se Lavoiser ve svém pojmenování mýlil, ale název byl do té doby příliš běžný na to, aby se změnil.
"Kyslík" se stal názvem v angličtině, přestože angličtí vědci byli proti.
Pozdější historie
Podle teorie atomů Johna Daltona mají všechny prvky jeden atom a atomy ve sloučeninách jsou obvykle osamocené. Například se mylně domníval, že voda (H2O) má vzorec pouze HO. V roce 1805 Joseph Louis Gay-Lussac a Alexander von Humboldt prokázali, že voda se skládá ze dvou atomů vodíku a jednoho atomu kyslíku. V roce 1811 Amedeo Avogadro na základě Avogadrova zákona správně určil, z čeho se voda skládá.
Koncem 19. století vědci zjistili, že vzduch lze stlačením a ochlazením přeměnit na kapalinu a izolovat v něm obsažené sloučeniny. Švýcarský chemik a fyzik Raoul Pictet objevil kapalný kyslík tak, že odpařováním oxidu siřičitého přeměnil oxid uhličitý na kapalinu. Ten pak také odpařoval, aby ochladil plynný kyslík a přeměnil jej na kapalinu. Dne 22. prosince 1877 zaslal Francouzské akademii věd telegram, v němž ji informoval o svém objevu.