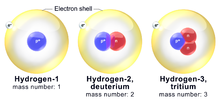
Atomy chemického prvku mohou existovat v různých typech. Ty se nazývají izotopy. Mají stejný počet protonů (a elektronů), ale různý počet neutronů. Různé izotopy téhož prvku mají různé hmotnosti. Hmotnost je výraz pro to, kolik látky (nebo hmoty) něco má. Věci s různou hmotností mají různou hmotnost. Protože různé izotopy mají různý počet neutronů, neváží všechny stejně a nemají stejnou hmotnost.
Různé izotopy téhož prvku mají stejné atomové číslo. Mají stejný počet protonů. O atomovém čísle rozhoduje počet protonů. Izotopy však mají různá hmotnostní čísla, protože mají různý počet neutronů.
Slovo izotop, které znamená na stejném místě, pochází ze skutečnosti, že izotopy se nacházejí na stejném místě v periodické tabulce prvků.
V neutrálním atomu se počet elektronů rovná počtu protonů. Izotopy stejného prvku mají také stejný počet elektronů a stejnou elektronickou strukturu. Protože o tom, jak se atom chová, rozhoduje jeho elektronická struktura, jsou izotopy chemicky téměř stejné, ale fyzikálně se liší od svých původních atomů.
Těžší izotopy reagují chemicky pomaleji než lehčí izotopy téhož prvku. Tento "hmotnostní efekt" je větší u procia (1H) a deuteria (2H), protože deuterium má dvakrát větší hmotnost než procium. U těžších prvků je relativní poměr atomových hmotností mezi izotopy mnohem menší a hmotnostní efekt je obvykle malý.
Jak se izotopy zapisují a jak spočítat počet neutronů
Izotopy se obvykle označují pomocí chemického symbolu doplněného o hmotnostní číslo A (součet protonů a neutronů), například 12C, 13C nebo 14C. Protonové číslo Z (počet protonů) určuje prvek; počet neutronů N lze spočítat jako N = A − Z. Například: uhlík-14 (14C) má A = 14, Z = 6, tedy N = 8 neutronů.
Typy izotopů
- Stabilní izotopy – nevyzařují radioaktivní záření a existují po neomezeně dlouhou dobu (např. 12C, 13C, 16O).
- Radioaktivní izotopy (radioizotopy) – jsou nestabilní a přeměňují se na jiné nuklidy vyzařováním částic či záření (alfa, beta, gama). Mají určitou poločas rozpadu (half-life), který udává, jak rychle se rozpadají (např. 14C, 3H).
Rozdíly v chemických a fyzikálních vlastnostech
Protože izotopy téhož prvku mají stejnou elektronovou konfiguraci, jsou jejich chemické vlastnosti velmi podobné. Přesto existují jemné rozdíly:
- Hmotnostní (izotopový) efekt – těžší izotopy vytvářejí silnější a méně „kmitající“ chemické vazby, což ovlivňuje rychlosti chemických reakcí (tzv. kinetický izotopový efekt). To je výrazné zejména u vodíku (protium vs. deuterium vs. tritium), kde rozdíl v hmotnosti výrazně mění reaktivity.
- Termodynamický efekt – rozdíly v nulové bodové energii vazeb mohou ovlivnit rovnovážné konstanty reakcí, takže poměry izotopů v produktech a reaktantech mohou být mírně odlišné.
- Fyzikální vlastnosti – hustota, bod tání a další fyzikální parametry se mohou u izotopů lišit kvůli rozdílné hmotnosti (např. těžká voda D2O má vyšší bod varu než H2O).
Příklady a aplikace
Praktická použití izotopů zahrnují:
- Datování – radioizotopy jako 14C se používají k datování organických materiálů (radiokarbonová metoda).
- Lékařství – radioizotopy (např. 99mTc, 131I) slouží k diagnostice a terapii v nukleární medicíně.
- Průmysl a výzkum – sledování procesů pomocí stopovacích izotopů, měření toků látek, analytické metody (hmotnostní spektrometrie).
- Energie – některé izotopy (např. 235U, 239Pu) jsou klíčové pro jaderné reakce v elektrárnách či ve zbraních; jiné (těžká voda) se používají jako moderátory v reaktorech.
- Ekologie a klimatologie – poměr stabilních izotopů (např. 18O/16O, 13C/12C) se používá ke studiu klimatu, potravních řetězců a zdrojů vody.
Další související pojmy
- Izotony – nuklidy s stejným počtem neutronů, ale různým počtem protonů.
- Isobary – nuklidy se stejným hmotnostním číslem A, ale různým Z.
- Izotopové poměry a průměrná atomová hmotnost – hodnota uvedená v periodické tabulce je průměr, který bere v úvahu přirozené zastoupení jednotlivých izotopů (vážený průměr).
Metody separace a bezpečnost
Rozdílné izotopy se mohou separovat centrifugací, difuzí, chemickými metodami nebo laserovými technikami (např. obohacování uranu). Radioaktivní izotopy vyžadují speciální bezpečnostní opatření při manipulaci a skladování kvůli riziku ionizujícího záření.
Stručné shrnutí
Izotopy jsou varianty stejných prvků s různým počtem neutronů, což vede k rozdílům v hmotnosti a některých fyzikálních vlastnostech. Chemicky jsou si velmi podobné díky stejné elektronové konfiguraci, ale hmotnostní rozdíly mohou ovlivnit rychlost a rovnováhu chemických reakcí. Izotopy mají široké využití v přírodních vědách, lékařství, průmyslu i v datování historických a geologických materiálů.