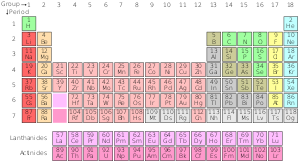
Periodická tabulka chemických prvků je seznam známých chemických prvků. V tabulce jsou prvky seřazeny podle svých atomových čísel počínaje nejnižším číslem jedna, vodíkem. Atomové číslo prvku je stejné jako počet protonů v daném jádru atomu. V periodické tabulce jsou prvky uspořádány do period a skupin. Řada prvků napříč tabulkou se nazývá perioda. Každá perioda má své číslo; od 1 do 8. V periodě 1 jsou pouze 2 prvky: vodík a helium. Období 2 a období 3 mají 8 prvků. Ostatní periody jsou delší. Prvky v periodě mají po sobě jdoucí atomová čísla.
Sloupec prvků v tabulce se nazývá skupina. Ve standardní periodické tabulce je 18 skupin. Každá skupina má své číslo: od 1 do 18. Prvky ve skupině mají elektrony uspořádány podobně, podle počtu valenčních elektronů, což jim dává podobné chemické vlastnosti (chovají se podobně). Například skupina 18 je známá jako vzácné plyny, protože všechny jsou plyny a neslučují se s jinými atomy.
Existují dva systémy číslování skupin; jeden používá arabské číslice (1,2,3) a druhý římské číslice (I, II, III). Římské číslice se používaly po většinu 20. století. V roce 1990 se Mezinárodní unie pro čistou a užitou chemii (IUPAC) rozhodla používat nový systém s arabskými číslicemi, který nahradil dva staré systémy skupin používající římské číslice.
Periodická tabulka slouží chemikům k pozorování zákonitostí a vztahů mezi prvky. Periodická tabulka obsahuje tři hlavní skupiny: kovy, metaloidy a nekovy. Například prvky úplně vlevo a dole v tabulce jsou nejvíce kovové a prvky vpravo nahoře jsou nejméně kovové. (Např. cesium je mnohem kovovější než helium). Existuje také mnoho dalších zákonitostí a vztahů.
Periodickou tabulku vynalezl ruský chemik Dmitrij IvanovičMendělejev (1834-1907). Na jeho počest byl po něm pojmenován prvek 101, mendelejev.