Kovalentní vazby jsou chemické vazby mezi dvěma nekovovými atomy, při nichž dochází ke sdílení valenčních elektronů. Příkladem je voda, kde vodík (H) a kyslík (O) tvoří vazbu (H2O). Cílem atomů při tvorbě vazeb je obvykle doplnit vnější slupku elektronů — plná vnější slupka má typicky osm elektronů (u vodíku a helia stačí dva). Valenční elektrony jsou ty, které se nacházejí ve vnějším obalu a podílejí se na chemických vazbách. Strukturu a rozložení těchto elektronů určuje kvantová mechanika a modely atomových orbitalů.
Počet elektronů v neutrálním atomu odpovídá počtu protonů v jádře. Elektrony se v kvantovém smyslu nevyrábějí jako přesné dráhy, ale jako rozložené pravděpodobnosti v orbitálech — lze to popsat i obrazně jako „rozmazané“ oblaky, které obklopují jádro (obíhají kolem je zjednodušený náhled). První elektronová vrstva může pojmout až dva elektrony, další obvykle až osm; právě ty vnější (valenční) jsou méně pevně vázány a účastní se vazeb. Kovalentní vazba vzniká tehdy, když si dva atomy sdílejí jeden nebo více párů valenčních elektronů tak, že tyto elektrony „patří“ všem zúčastněným atomům současně.
Vznik vazby lze vysvětlit i energeticky: při přiblížení dvou atomů se mohou překrývat jejich atomové orbitaly a vznikne společný molekulový orbital o nižší energii než původní samostatné orbitaly. Elektron může tento nový, energeticky výhodnější orbital obsadit a soustava tak uvolní přebytečnou energii (např. vyzářením fotonu). Nižší energie znamená stabilnější stav a tím i vznik vazby. V kovalentní vazbě mezi atomy stejného prvku (např. H–H, Cl–Cl) se elektrony sdílejí rovnoměrně (nepolarita). Pokud mají atomy odlišnou schopnost vázat elektrony (elektronegativitu), elektronový pár se posunuje více k tomu elektronegativnějšímu atomu a vznikají částečné (parciální) náboje: atom s vyšší elektronegativitou získá částečný záporný náboj (δ−) a druhý atom částečný kladný (δ+). To je základ polarit kovalentních vazeb.
Typy kovalentních vazeb a jejich vlastnosti
- Jednoduchá vazba – sdílení jednoho páru elektronů (např. H–H, C–H). Vzniká typicky sigma (σ) vazba.
- Dvojná vazba – sdílení dvou párů elektronů (např. O=O, C=C) složená z jedné σ a jedné π vazby; je kratší a silnější než jednoduchá.
- Trojitá vazba – sdílení tří párů elektronů (např. N≡N), obsahuje jednu σ a dvě π vazby; je ještě kratší a pevnější.
- Sigma (σ) a pí (π) vazby – σ vzniká přímým překryvem orbitalů podél spojnice jader, π vzniká vedlejším překryvem nad a pod touto spojnicí.
- Polarita – rozdíl elektronegativity určuje, zda je vazba nepolární (rovnoměrné sdílení) nebo polární (nerovnoměrné sdílení se vznikem δ+ a δ−).
- Směrnost – kovalentní vazby jsou směrové (molekula má konkrétní geometrii), na rozdíl od iontové vazby, která je nerychlostní v krystalu.
Vazebná energie a délka
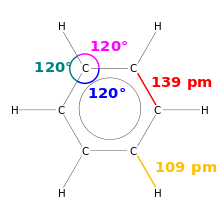
Vazebná energie (energie potřebná k rozbití vazby) i délka vazby závisí na typu vazby a na prvcích, které se podílejí. Obecně platí: silnější vazba → vyšší vazebná energie → kratší délka vazby. Například trojná vazba má vyšší energii a kratší délku než dvojná, a ta zase více než jednoduchá.
Struktury (Lewis), hybridizace a tvar molekul
Pro jednoduché znázornění kovalentních vazeb se používají Lewisovy struktury, kde jsou valenční elektrony zakresleny jako tečky a vazby jako čáry. Kvantově‑chemické vysvětlení tvaru molekul zahrnuje hybridizaci orbitalů (např. sp, sp2, sp3) a také model VSEPR (valence shell electron pair repulsion), který popisuje, jak se páry elektronů (vazebné i volné) rozmístí, aby se vzájemně odpuzovaly co nejméně.
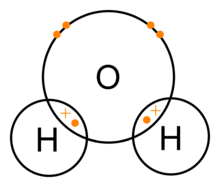
Voda (H2O) – konkrétní příklad
Molekula vody se skládá z jednoho atomu kyslíku a dvou atomů vodíku. V jednoduchém pojetí kyslík s každým atomem vodíku sdílí jeden elektronový pár (dva páry celkem), čímž každému vodíku vznikne stabilní duplet a kyslíku se přibližně doplní oktet. Kyslík má navíc ještě dva nepřipojené (volné) elektronové páry. Podle hybridizace atomu kyslíku jde v molekule vody o sp3 hybridizaci: čtyři sp3 orbitaly — dvě obsahují vazebné páry O–H a dvě obsahují volné páry.
Důsledkem uspořádání těchto párů je, že molekula vody není lineární, ale ohnutá (tzv. „bent“) s vazebným úhlem přibližně 104,5°. Protože kyslík je výrazně více elektronegativní než vodík, sdílené elektronové páry jsou posunuté blíže ke kyslíku. To dává kyslíku částečný záporný náboj (δ−) a každému vodíku částečný kladný náboj (δ+). V důsledku této nerovnoměrné distribuce elektronů je molekula vody polární — její elektrický náboj není rozložen rovnoměrně.
Polární charakter vody má dalekosáhlé následek: mezi molekulami vody vznikají silné mezimolekulární vodíkové vazby (H…O), které vysvětlují vysoké bodu varu a tání vůči molekulové hmotnosti, vysoké povrchové napětí, dobrou rozpustnost mnoha polárních látek a další unikátní vlastnosti vody jako rozpouštědla života.
Krátké shrnutí
- Kovalentní vazba vzniká sdílením valenčních elektronů mezi atomy a vede k vytvoření stabilnějších molekul.
- Vazby mohou být nepolární (rovnoměrné sdílení) nebo polární (nerovnoměrné sdílení), závisí na elektronegativitě prvků.
- Molekula vody je příkladem polární kovalentní vazby: kyslík nese částečný záporný náboj, vodíky částečné kladné, a výsledkem je bent tvar VSEPR a vznik vodíkových vazeb mezi molekulami.
- Kovalentní vazby jsou směrové, jejich síla a délka závisí na počtu sdílených elektronových párů a typu orbitalového překryvu (σ, π).