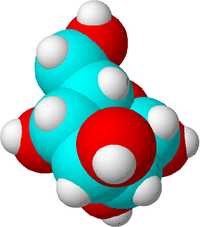
Molekula je nejmenší množství chemické látky, které může existovat. Kdyby se molekula rozdělila na menší části, jednalo by se o jinou látku.
Molekuly se skládají z atomů, které jsou k sobě přilepeny v určitém tvaru nebo formě. Ne všechny kombinace atomů jsou stejně možné; atomy vytvářejí určité tvary přednostně před jinými. Také mají různou valenci. Například atomy kyslíku mají vždy dvě vazby s jinými atomy, atomy uhlíku mají vždy čtyři vazby s jinými atomy a atomy dusíku mají vždy tři vazby s jinými atomy.
V kinetické teorii plynů se termín molekula často používá pro jakoukoli plynnou částici bez ohledu na její složení. Podle této definice jsou atomy vzácných plynů považovány za molekuly, protože jsou ve skutečnosti jednoatomovými molekulami.
V plynech, jako je vzduch, molekuly jen poletují. V kapalinách, jako je voda, jsou molekuly přilepené k sobě, ale mohou se pohybovat. V pevných látkách, jako je cukr, mohou molekuly pouze vibrovat. Ve čtvrtém stavu hmoty, známém jako plazma, jsou atomy ionizované a nemohou tvořit molekuly.
Pomocí molekulového vzorce můžete zapsat čísla všech atomů v molekule. Například molekulový vzorec glukózy je C6H12O6. To znamená, že jedna molekula glukózy se skládá ze šesti atomů uhlíku, dvanácti atomů vodíku a šesti atomů kyslíku.