Ve vesmíru existují čtyři běžné stavy hmoty (nebo fáze): pevná látka, kapalina, plyn a plazma. Stav hmoty ovlivňuje vlastnosti látky, jako je hustota, viskozita (jak dobře teče), poddajnost (jak snadno se ohýbá) a vodivost.
Krátké vysvětlení
Stav hmoty popisuje, jak jsou částice (atomy, molekuly, ionty) uspořádány a jak se pohybují. Změna teploty nebo tlaku často mění i stav hmoty — například táním pevná látka přechází v kapalinu, nebo při zahřívání kapalina přechází v plyn. Klasické čtyři stavy — pevné, kapalné, plynné a plazma — pokrývají většinu běžných situací, ale existují i exotické fáze, o kterých níže.
Charakteristika základních stavů
- Pevné látky: částice jsou v pevné nebo pravidelné mřížce (u krystalických látek) nebo v neuspořádaném, ale pevně vázaném stavu (u amorfních pevných látek). Mají tvar i objem téměř konstantní, vysokou hustotu a malou stlačitelnost. Mechanické vlastnosti zahrnují pevnost, tvrdost a křehkost nebo tažnost.
- Kapaliny: mají téměř stálý objem, ale přijímají tvar nádoby. Částice se mohou vzájemně klouzat, proto kapaliny tečou; síly mezi částicemi jsou střední. Kapaliny mají vyšší hustotu než plyny a výraznou viskozitu (od tekutého medu po vodu).
- Plyny: částice se pohybují volně a jsou velice vzdálené, mezičásticové síly jsou zanedbatelné. Plyny vyplňují celý dostupný objem, jsou snadno stlačitelné a mají nízkou hustotu. Chování plynů často popisuje stavová rovnice (např. ideální plyn).
- Plazma: ionizovaný plyn obsahující volné elektrony a ionty; chová se elektricky vodivě a reaguje na elektromagnetické pole. Plazma vzniká při vysokých teplotách nebo za intenzivního ionizačního záření. Příklady: slunce a hvězdy, blesky, některé druhy výbojek a uměle vytvořená plazma v laboratorních podmínkách.
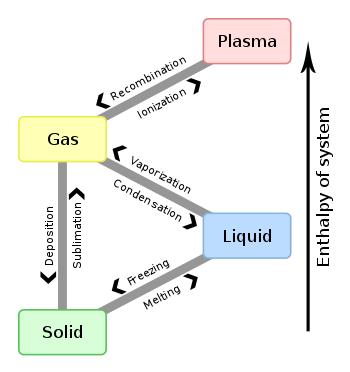
Přechody mezi stavy (fázové změny)
- Tání (pevné → kapalné) a tuhnutí (kapalné → pevné).
- Vypařování (kapalné → plynné) a kondenzace (plynné → kapalné); var je rychlé vypařování v celém objemu kapaliny.
- Sublimace (pevné → plynné) a desublimace nebo resublimace (plynné → pevné) — např. suchý led (CO2) sublimuje přímo do plynu.
- Ionizace (plyn → plazma) a rekombinace (plazma → plyn).
Tyto přechody závisí na teplotě a tlaku; často je znázorňujeme pomocí fázového diagramu látky, kde najdeme např. bod tání, varu a kritický bod (kde se rozdíl mezi kapalinou a plynem vytrácí a vzniká superkritická fáze).
Další, méně běžné nebo exotické stavy
- Superkritická kapalina: vzniká při teplotě a tlaku nad kritickým bodem; má vlastnosti mezi kapalinou a plynem. Využití: extrakce (superkritické CO2).
- Bose‑Einsteinův kondenzát (BEC): vzniká při extrémně nízkých teplotách, kdy bosony obsadí stejný kvantový stav a látka vykazuje makroskopické kvantové jevy (superfluidita, koherence).
- Fermionické kondenzáty, kvantové kapaliny, supravodivost a superfluidita: speciální kvantové fáze s unikátními vlastnostmi proudění a vodivosti.
- Amorfní pevné látky (skla): nemají krystalickou mřížku a chovají se někde mezi pevnou látkou a viskózní kapalinou při dlouhých časových měřítkách.
Fyzikální vlastnosti a praktické příklady
Stav hmoty určuje mnoho naměřitelných veličin:
- Hustota: pevné látky > kapaliny > plyny (obecně), ale jsou výjimky (např. led je méně hustý než voda).
- Viskozita: určuje odpor proti proudění u kapalin a plynů.
- Elektrická a tepelná vodivost: plazma a některé kovové pevné látky vedou elektřinu dobře; izolátory nevedou.
- Stlačitelnost: plyny jsou snadno stlačitelné, kapaliny a pevné látky téměř nikoli.
Příklady z praxe: voda je kapalina používaná v mnoha procesech; vzduch je směs plynů; železo v pevné formě tvoří konstrukce; plazma je v luminiscenčních trubicích, výbojkách a v kosmických objektech.
Proč je to důležité
Pochopení stavů hmoty je klíčové v materiálovém inženýrství, chemii, fyzice, meteorologii i v kosmologii. Volba stavu a řízení fázových přechodů umožňuje navrhovat materiály s požadovanými vlastnostmi, optimalizovat technologické procesy (např. separace, sušení, lisování) a vysvětlovat přírodní jevy — od mraků na Zemi po chování hvězd ve vesmíru.