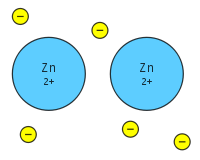
Kovová vazba je sdílení mnoha oddělených elektronů mezi mnoha kladnými ionty, přičemž elektrony působí jako "lepidlo", které dává látce určitou strukturu. Na rozdíl od kovalentní nebo iontové vazby. Kovy mají nízkou ionizační energii. Proto mohou být valenční elektrony delokalizovány v rámci kovů. Delokalizované elektrony nejsou spojeny s konkrétním jádrem kovu, místo toho se mohou volně pohybovat po celé krystalické struktuře a vytvářejí "moře" elektronů.
Mezi elektrony a kladnými ionty kovu působí silná přitažlivá síla. Proto mají kovy často vysoké teploty tání nebo varu. Princip je podobný jako u iontových vazeb.
Kovové vazby jsou příčinou mnoha vlastností kovů, jako je pevnost, kujnost, tažnost, lesk, vedení tepla a elektřiny.
Protože se elektrony volně pohybují, má kov určitou elektrickou vodivost. Díky ní může energie rychle procházet elektrony a vytvářet elektrický proud. Kovy vedou teplo ze stejného důvodu: volné elektrony mohou přenášet energii rychleji než jiné látky s elektrony, které jsou pevně usazeny na svých místech. Existuje také několik nekovů, které vedou elektrický proud: grafit (protože má stejně jako kovy volné elektrony) a iontové sloučeniny, které jsou roztavené nebo rozpuštěné ve vodě a které mají volně se pohybující ionty.
Kovové vazby mají alespoň jeden valenční elektron, který nesdílejí se sousedními atomy, a neztrácejí elektrony za vzniku iontů. Místo toho se vnější energetické hladiny (atomové orbitaly) atomů kovů překrývají. Jsou podobné kovalentním vazbám. Ne všechny kovy vykazují kovovou vazbu. Například ionty rtuti (Hg2+
2) tvoří kovalentní vazby kov-kov.
Slitina je roztok kovů. Většina slitin je lesklá stejně jako čisté kovy.