Atomové orbitaly jsou místa v okolí jádra atomu, kde se v daném okamžiku s největší pravděpodobností nacházejí elektrony. Jedná se o matematickou funkci, která popisuje vlnové chování jednoho elektronu nebo dvojice elektronů v atomu.
Slovo "orbitální" se používá proto, že se předpokládalo, že elektrony se chovají podobně jako sluneční soustava, kde jádro je jako Slunce a elektrony obíhají jako planety.
Počet atomových orbitalů v prvku je dán periodou, ve které se prvek nachází. Elektrony se pohybují mezi orbitaly v závislosti na tom, jak rychle se pohybují a kolik dalších elektronů se v nich nachází.
V atomové teorii a kvantové mechanice je atomový orbital kvantovým číslem. Každý takový orbital může být obsazen jedním nebo dvěma elektrony. Způsob uspořádání orbitalů souvisí s elektronovými konfiguracemi atomů. Byly odvozeny z popisů, které poskytli dřívější spektroskopové některých spektroskopických čar alkalických kovů jako ostré, hlavní, rozptýlené a základní.
Kvantová čísla a základní vlastnosti orbitalů
Každý atomový orbital je charakterizován třemi (čtyřmi včetně spinu) kvantovými čísly:
- Hlavní kvantové číslo n (n = 1, 2, 3, ...) určuje energii a velikost orbitalu — čím větší n, tím dál je elektron v průměru od jádra.
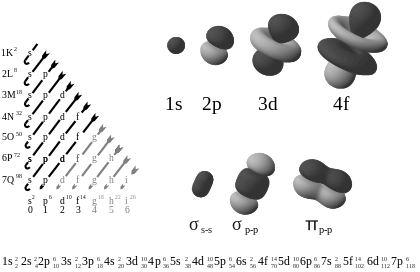
- Vedlejší (orbitální) kvantové číslo l (l = 0, 1, ..., n−1) určuje tvar orbitalu. Hodnoty l se označují písmeny: l = 0 → s, l = 1 → p, l = 2 → d, l = 3 → f.
- Magnetické kvantové číslo m (m = −l, −l+1, ..., 0, ..., +l) určuje orientaci orbitalu v prostoru (např. tři p-orbitaly px, py, pz odpovídají m = −1, 0, +1).
- Spinové kvantové číslo ms (ms = +1/2 nebo −1/2) popisuje spin elektronu; v jednom orbitalu mohou být maximálně dva elektrony s opačnými spiny (Pauliho vylučovací princip).
Tvary orbitalů a počet uzlů
S-orbitaly (l = 0) mají sférickou symetrii. P-orbitaly (l = 1) mají tvar s dvěma laloky oddělenými uzlovou rovinou. D- a f-orbitaly mají složitější tvary s několika laloky a uzlovými plochami. Počet radiálních a úhlových uzlů roste s n a l — uzlové plochy jsou místa, kde je pravděpodobnost nalezení elektronu nulová.
Obsazování orbitalů a pravidla
Elektrony zaplňují orbitaly podle několika pravidel:
- Aufbau princip – orbitaly se obsazují od nejnižší energie směrem vzhůru.
- Pauliho vylučovací princip – žádné dva elektrony v atomu nemohou mít stejnou sadu všech čtyř kvantových čísel; v jednom orbitalu tedy mohou být nejvýše dva elektrony s opačnými spiny.
- Hundovo pravidlo – při obsazování degnerovaných orbitalů (stejné energie, např. tři p-orbitaly) preferují elektrony nejprve obsazení každého orbitalu jedním elektronem se stejným spinem, než začnou pár tvořit.
Energetické uspořádání a periodicita
Pořadí energií orbitalů (např. 1s < 2s < 2p < 3s < 3p < 4s < 3d < 4p atd.) určuje, jaké orbitaly jsou obsazeny u různých prvků a vysvětluje periodické vlastnosti prvků. U těžších prvků se pořadí může měnit kvůli relativistickým efektům a interakcím mezi elektrony.
Vizualizace orbitálů
Atomové orbitaly jsou často znázorňovány pomocí izoploš (ploch stejné hustoty elektronového oblaků). Tyto obrazy ukazují oblasti vysoké pravděpodobnosti nalezení elektronu (laloky) a uzlové plochy. Moderní počítačové metody (např. Hartree–Fock, DFT) poskytují kvantitativní tvary a energie orbitalů.
Význam orbitalů v chemii a fyzice
- Chemické vazby: Tvar a energie valenčních orbitalů určují, jak atomy tvoří kovalentní nebo koordinační vazby (např. překrytí orbitálů při tvorbě σ a π vazeb).
- Spektroskopie: Přechody elektronů mezi orbitaly vysvětlují spektrální čáry, jejich polohu a intenzitu (odkazy v původním textu k historickým spektrům alkalických kovů).
- Reaktivity a katalýza: Elektronová konfigurace a obsazenost orbitalů ovlivňují reaktivitu atomů a molekul, jejich acidobazické vlastnosti a katalytické chování.
- Materiálové vlastnosti: Vlastnosti polovodičů, magnetismus nebo chemické vazby v pevných látkách často závisí na uspořádání elektronů v orbitalech (např. delokalizované orbitály v kovech nebo π-systémech).
Krátké shrnutí
Atomové orbitaly nejsou pevné dráhy elektronů, ale matematické funkce, které dávají pravděpodobnost, kde se elektron v atomu nachází. Jejich tvar, energie a obsazení řízené kvantovými čísly vysvětlují periodické vlastnosti prvků, vznik chemických vazeb a mnohé spektroskopické i materiálové jevy.