V chemii a fyzice vysvětluje atomová teorie, jak se v průběhu času měnilo naše chápání atomu. Kdysi byly atomy považovány za nejmenší části hmoty. Nyní je však známo, že atomy se skládají z protonů, neutronů a elektronů. Tyto subatomární částice se skládají z kvarků. S první myšlenkou atomu přišel řecký filozof Démokritos. Mnoho myšlenek moderní teorie pochází od Johna Daltona, britského chemika a fyzika.
Teorie platí pro pevné látky, kapaliny a plyny, ale neplatí obdobně pro plazma nebo neutronové hvězdy.
Co je atomová teorie
Atomová teorie je souhrn myšlenek a modelů, které popisují vnitřní stavbu atomů, jejich chování, stabilitu a vzájemné interakce. Nejde o jednu neměnnou „teorii“ v jediném smyslu, ale o historicky vyvíjený soubor modelů — od jednoduchých představ až po kvantově-mechanické popisy, které dnes vysvětlují chemické vlastnosti prvků a výsledky experimentů.
Krátká historie a hlavní modely
- Démokritos (antika) – představil pojem „atomos“ jako nedělitelnou částici hmoty (filozofická myšlenka bez experimentálního podkladu).
- John Dalton (počátek 19. století) – oživuje atomy v chemii: navrhl, že prvky jsou tvořeny určitými druhy atomů s charakteristickou hmotností, které se spojují v poměrech v chemických reakcích.
- J. J. Thomson – po objevu elektronu navrhl tzv. „plum pudding“ model, kde byly záporné elektrony rozptýleny v kladném „oblačí“.
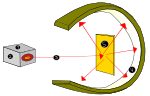
- Ernest Rutherford – pokusy s prozařováním zlaté fólie vedly k závěru, že většina hmoty a kladného náboje je soustředěna v malém jádře (planetární model jádra a oblak elektronů).
- Niels Bohr – navrhl kvantované energetické hladiny pro elektrony kolem jádra, což vysvětlovalo spektrální čáry vodíku.
- Kvantově-mechanický model (Schrödinger, Heisenberg atd.) – elektrony nejsou malé „planety“, ale kvantové vlnové funkce, které dávají pravděpodobnostní rozložení (orbitaly) a pravidla pro jejich obsazení (Pauliho princip).
Struktura atomu
- Jádro – obsahuje protony (kladný náboj) a neutrony (elektricky neutrální). Jádro nese téměř veškerou hmotnost atomu a je v něm koncentrována kladná část náboje.
- Elektronový obal – tvořen elektrony uspořádanými do orbitalů a elektronových hladin. Elektrony určují chemické vlastnosti a vazby mezi atomy.
- Substruktura částic – protony a neutrony jsou složeny z kvarků (především up a down kvarky) vázaných silnými interakcemi zprostředkovanými gluony.
Základní pojmy a veličiny
- Atomové číslo (Z) – počet protonů v jádře; určuje identitu prvku (např. Z = 6 znamená uhlík).
- Hmotnostní číslo (A) – součet protonů a neutronů; určuje nuklid a přispívá k atomové hmotnosti.
- Izotopy – atomy téhož prvku s různým počtem neutronů (např. 12C a 14C mají stejné Z, liší se A).
- Ionty – atomy s nerovnováhou mezi protony a elektrony (kladné nebo záporné náboje) vznikají ztrátou nebo přijetím elektronů.
Experimentální důkazy
Vývoj atomové teorie byl podložen řadou experimentů: pozorování spektrálních čar (spektra), experimenty s katodovými paprsky (objev elektronu), Rutherfordův rozptyl částic na zlaté fólii (objev jádra), rozvoj hmotnostních spektrometrů (měření izotopů) a mnoho dalších moderních technik (snímání jadernou magnetickou rezonancí, urychlovače částic, elektronová mikroskopie, rozptyl a spektroskopie v synchrotronech).
Veličiny, měřítka a stabilita
Typický atom má průměr přibližně 0,1–0,5 nm (10^−10 m) a jádro má rozměr řádově 10^−15 m — tedy mnohem menší, ale hustší. Hmotnosti se udávají v atomových hmotnostních jednotkách (u), kde 1 u ≈ 1/12 hmotnosti 12C. Stabilita atomu závisí na poměru protonů a neutronů v jádře; některé kombinace vedou k radioaktivnímu rozpadu.
Kdy atomová teorie nepostačuje
Popis atomů pomocí běžných atomových modelů neplatí v extrémních podmínkách. Například v plazmě jsou elektrony oddělené od jader a chování určuje kolektivní elektrické a magnetické interakce. V extrémních hustotách, jako jsou neutronové hvězdy, mohou být neutrony a další částice stlačeny do stavů, které běžné atomové modely nepokrývají.
Význam pro chemii a fyziku
Atomová teorie je základem chemie (vysvětluje vazby, strukturu molekul, reaktivity) i fyziky (jádrová fyzika, částicová fyzika, materiálové vědy). Moderní technologie — polovodiče, lékařské zobrazování, jaderná energie či syntéza nových prvků — vycházejí z aplikací poznatků o struktuře atomů.
Závěr
Atomová teorie je dynamický a ověřovaný soubor modelů, které vysvětlují vnitřní stavbu hmoty od elementárních částic až po chemické vlastnosti. Díky kombinaci experimentů a teorie (klasické i kvantové) dnes dokážeme popsat většinu jevů v běžných podmínkách, zároveň však zůstávají oblasti s extrémními parametry, kde je třeba uplatnit speciální fyzikální přístupy.