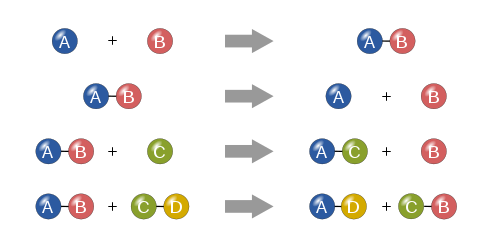
Syntéza
Při syntézní reakci se dvě nebo více jednoduchých látek spojí za vzniku složitější látky.
A + B ⟶ A B {\displaystyle A+B\podlouhlá pravá šipka AB} 
"Dva nebo více reaktantů dává jeden produkt" je další způsob, jak identifikovat syntézní reakci. Příkladem syntézní reakce je kombinace železa a síry za vzniku sulfidu železa(II):
8 F e + S 8 ⟶ 8 F e S {\displaystyle 8Fe+S_{8}\longrightarrow 8FeS} 
Dalším příkladem je jednoduchý plynný vodík kombinovaný s jednoduchým plynným kyslíkem za vzniku složitější látky, například vody.
Rozklad
Rozkladná reakce probíhá tak, že se složitější látka rozkládá na jednodušší části. Je to tedy opak syntézy a lze ji zapsat jako:
A B ⟶ A + B {\displaystyle AB\podlouhlá pravá šipka A+B} 
Příkladem rozkladné reakce je elektrolýza vody za vzniku kyslíku a plynného vodíku:
2 H 2 O ⟶ 2 H 2 + O 2 {\displaystyle 2H_{2}O\longrightarrow 2H_{2}+O_{2}}} 
Jediná výměna
Při jednoduché náhradní reakci nahrazuje jeden nekombinovaný prvek jiný prvek ve sloučenině; jinými slovy, jeden prvek si vymění místo s jiným prvkem ve sloučenině Tyto reakce mají obecně podobu:
A + B C ⟶ A C + B {\displaystyle A+BC\longrightarrow AC+B} 
Příkladem jednoduché vytěsňovací reakce je reakce, při níž hořčík nahrazuje vodík ve vodě za vzniku hydroxidu hořečnatého a plynného vodíku:
M g + 2 H 2 O ⟶ M g ( O H ) 2 + H 2 {\displaystyle Mg+2H_{2}O\longrightarrow Mg(OH)_{2}+H_{2}} 
Dvojitá výměna
Při reakci dvojné záměny si anionty a kationty dvou sloučenin vymění místa a vytvoří dvě zcela odlišné sloučeniny. Tyto reakce mají obecný tvar:
A B + C D ⟶ A D + C B {\displaystyle AB+CD\longrightarrow AD+CB} 
Například při reakci chloridu barnatého (BaCl2 ) a síranu hořečnatého (MgSO4 ) si anion SO42− vymění místo s anionem 2Cl−, čímž vzniknou sloučeniny BaSO4a MgCl 2.
Dalším příkladem reakce dvojího vytěsnění je reakce dusičnanu olovnatého(II) s jodidem draselným za vzniku jodidu olovnatého(II) a dusičnanu draselného:
P b ( N O 3 ) 2 + 2 K I ⟶ P b I 2 + 2 K N O 3 {\displaystyle Pb(NO_{3})_{2}+2KI\longrightarrow PbI_{2}+2KNO_{3}}}