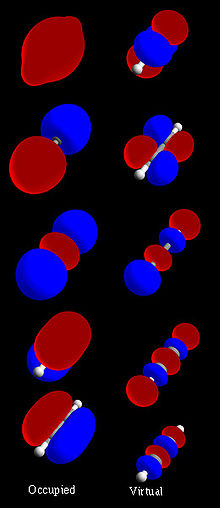
V chemii molekulový orbital (neboli MO) vysvětluje, co se děje s elektrony, když se atomy spojí v molekule. MO je matematická funkce, která popisuje vlnové chování elektronu v molekule. Chemici tyto funkce používají k předpovídání nebo vysvětlování chemických a fyzikálních vlastností. Funkce mohou například říci, jaká je pravděpodobnost, že se elektron nachází v nějaké konkrétní oblasti.
Chemici obvykle sestavují matematické modely molekulových orbitalů kombinací atomových orbitalů. Lze také použít hybridní orbitaly z každého atomu molekuly nebo jiné molekulové orbitaly ze skupin atomů. S těmito funkcemi mohou pracovat počítače. Molekulární orbitaly umožňují chemikům aplikovat kvantovou mechaniku při studiu molekul. MO odpovídají na otázky, jak atomy v molekulách drží pohromadě. Různé zaoblené tvary v orbitálním diagramu označují, kde by se v atomu nejspíše nacházely elektrony.
Základní princip: LCAO a superpozice
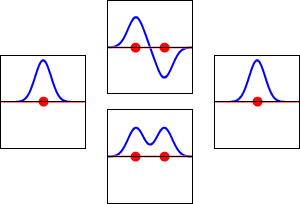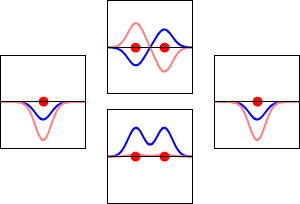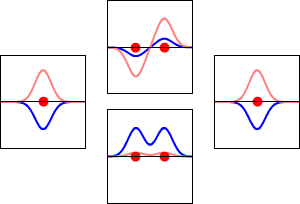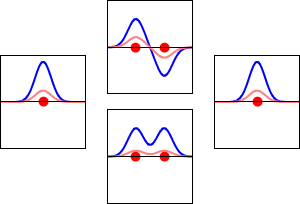
Jednoduchý způsob, jak vznikají molekulové orbitaly, je metoda LCAO (linear combination of atomic orbitals) – lineární kombinace atomových orbitalů. Když se dva atomové orbitaly navzájem kombinují, vznikají dva výsledné molekulární orbitaly:
- vazebný orbital (bonding) – amplitudy vlnových funkcí mají stejný smysl, dochází k zvětšení elektronové hustoty mezi jádry a k energetickému snížení;
- protivazebný orbital (antibonding) – amplitudy mají opačný smysl, mezi jádry vzniká uzel a orbital má vyšší energii.
Kromě toho může vzniknout neutrální (nonbonding) orbital, jehož energie a tvar jsou podobné původnímu atomovému orbitalu a který výrazně neovlivňuje vazbu.
Typy molekulových orbitalů
- Sigma (σ) – vznikají podél osy spojující jádra; často z 1s, sp nebo pz orbitalů; mají kruhovou symetrii kolem osy vazby.
- Pi (π) – vznikají z bočního překrytí p orbitalů; mají uzly na ose mezi jádry a charakteristickou dvoulobou symetrii.
- Delta (δ) – raritnější, vyskytují se u některých přechodných kovů (překrytí d orbitalů).
Obsazování orbitalů a pravidla
Elektrony v molekulových orbitalech se řídí stejnými kvantovými pravidly jako v atomech:
- Paulího vylučovací princip – v jednom orbitalu mohou být maximálně dva elektrony s opačnými spiny.
- Hundovo pravidlo – u orbitalů stejné energie se elektrony obsazují s paralelními spiny, pokud je to možné.
- Pořadí energií orbitalů závisí na molekule; pro jednoduché diatomické molekuly je často ukazováno v MO diagramech (např. pro H2, He2, Li2, ...).
Vazebný řád lze odhadnout podle počtu elektronů v vazebných (nbonding) a protivazebných (nantibonding) orbitalech pomocí výrazu:
vazebný řád = (nbonding − nantibonding) / 2
HOMO, LUMO a reaktivita
Nejvyšší obsazený molekulový orbital se označuje HOMO (Highest Occupied Molecular Orbital) a nejnižší volný orbital LUMO (Lowest Unoccupied Molecular Orbital). Energie a složení HOMO a LUMO hrají klíčovou roli v chemické reaktivitě, fotochemii a spektru molekuly. Malý rozdíl energie HOMO–LUMO obvykle znamená vyšší reaktivitu a absorpci světla při delším vlnovém délkovém rozsahu (nižší energetické excitace).
Příklady a důsledky v praxi
- H2: jednoduchý případ, kde kombinace dvou 1s orbitalů dává vazebný σ1s a protivazebný σ*1s; obsazením dvou elektronů v σ1s vzniká stabilní jednostranná vazba.
- O2: má v MO diagramu dva nespárované elektrony v π* (antibonding) orbitalech, což vysvětluje paramagnetické chování kyslíku.
- N2: vysoký vazebný řád (trojná vazba) – pevná a krátká vazba, malé reaktivita vůči běžným činidlům.
- Benzén: delokalizované π orbitaly nad a pod rovinou kruhu vedou k aromatické stabilizaci a specifickým spektrálním vlastnostem.
Výpočtové metody a interpretace
Popis MO se provádí analyticky i numericky. Mezi běžné výpočetní metody patří:
- Hartree–Fock (HF) – základní kvantově-chemická metoda, která používá jednoelektronové orbitaly a průměrný elektrostatický efekt elektronů;
- DFT (density functional theory) – velmi používaná metoda pro výpočty elektronové hustoty a energetických vlastností s dobrým poměrem přesnost / výpočetní náročnost;
- post‑Hartree–Fock (MP2, CI, CCSD(T) apod.) – zahrnují korelace elektronů a poskytují vyšší přesnost za cenu vyšší výpočetní náročnosti.
Počítače a vizualizační programy umožňují kreslit tvary MO, izoplochy elektronové hustoty a energetické diagramy. Tyto obrazy pomáhají pochopit, kde se elektron nachází a jak orbitaly ovlivňují vlastnosti molekuly.
Význam v chemii a aplikace
Molekulární orbitaly jsou zásadní pro pochopení a predikci:
- typů a síly chemických vazeb,
- magnetických vlastností (paramagnetismus vs. diamagnetismus),
- spektrálních přechodů (UV/VIS, fotochemie),
- reaktivity a mechanizmů organických reakcí (fronty HOMO/LUMO),
- materiálových vlastností, katalýzy a navrhování nových molekul v chemii a farmacii.
Tipy pro studenty
- Začněte jednoduchými příklady (H2, He2, Li2, Be2, B2, C2, N2, O2, F2) a sledujte, jak se mění MO diagram při zvyšujícím se počtu elektronů.
- Procvičujte výpočet vazebného řádu a určování paramagnetismu podle obsazení π* orbitalů.
- Využívejte vizualizační nástroje k zobrazení tvarů orbitalů – obraz často pomůže pochopit abstraktní matematiku.
Celkově jsou molekulární orbitaly mocným rámcem, který propojuje kvantovou mechaniku s pozorovatelnými chemickými vlastnostmi a poskytuje praktické nástroje pro výzkum i výuku.