Definice
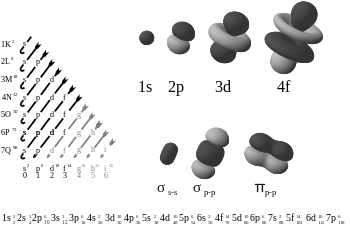
V chemii jsou vazby typu pí (π) kovalentní chemické vazby, při kterých se dráha (fáze) jednoho orbitalu překrývá bočně s dráhou druhého orbitalu. Typicky jde o boční překrytí dvou p‑orbitalů, jejichž laloky mají tvar „osmičky“ a vytvářejí dvě oblasti překrytí (nad a pod osou vazby). V důsledku toho existují dvě zóny elektronového hustoty. Pouze jedna z uzlových rovin orbitalu prochází oběma zúčastněnými jádry, což je typické rozlišení oproti sigma (σ) vazbám.
Vznik vazby π
Řecké písmeno π v názvu odkazuje na p‑orbitaly (řecké písmeno). Vazba π vzniká postranním (bočním) překrytím dvou p‑orbitalů, které jsou navzájem paralelní a kolmé na osu spojující jádra. Pokud se orbitály dotýkají s opačnou fází, vzniká antibondingový π* orbital. Symetrie orbitalů vazby π při pohledu podél osy vazby odpovídá tvaru p‑orbitalů; proto jsou p‑orbitaly hlavním zdrojem tohoto typu vazby.
U těžších atomů mohou též hrát roli d‑orbitaly a v literatuře se někdy připouští d‑přínos k vazbě π (např. u prvků 3. periody). Moderní vysvětlení hypervalence však často méně spoléhá na aktivní zapojení d‑orbitalů a více na rezonanční a iontové přispění k vazbě.
Porovnání s vazbou σ
Vazby π jsou obvykle slabší než vazby sigma. Z kvantově mechanického pohledu je důvod jednoduchý: boční překrytí p‑orbitalů je menší než přímé překrytí, které vytváří σ‑vazbu, takže výsledná energie vazby je nižší. Proto se π‑vazba snadněji přerušuje než σ‑vazba a π‑elektrony jsou často chemicky reaktivnější.
Vlastnosti vazeb π
- Rozložení elektronů: Elektronová hustota je soustředěna nad a pod osou vazby (dvě oblasti překrytí).
- Nedovolují volnou rotaci: Molekulární fragmenty spojené vazbou π se nemohou libovolně otáčet kolem osy vazby, aniž by se vazba nezničila — rotace naruší paralelní orientaci p‑orbitalů a proto rozbije π překrytí.
- Energetické hladiny: Základní (bonding) π orbital má nižší energii než jednotlivé atomové p‑orbitaly; jeho excitovaný protějšek je antibondingový π* orbital, důležitý pro spektroskopii a reakční mechanismy.
- Reaktivita: π‑elektrony jsou obvykle výše energeticky než σ‑elektrony a tvoří HOMO v mnoha nenasycených sloučeninách — to je důvod, proč jsou π‑systémy náchylné k elektrofilním reakcím (např. adice na alkeny).
- Konjugace a delokalizace: Když jsou π‑orbitaly na sousedních atomech navzájem paralelní a překrývají se, může vzniknout konjugovaný systém s delokalizovanými π‑elektrony (nižší celková energie, speciální optické a elektronové vlastnosti).
Molekulové orbitaly a spektrální důsledky
V rámci molekulové orbitalové teorie se z kombinace atomových p‑orbitalů tvoří vazebné π a odpudivé π* orbitaly. Rozdíl energie mezi těmito hladinami (HOMO–LUMO) určuje absorpce v UV‑vis spektru — konjugované systémy vykazují posun absorpce do delších vlnových délek. V infračervené spektroskopii má např. C=C vazba charakteristický absorpční pás okolo 1600–1680 cm−1.
Příklady
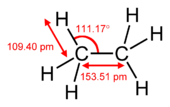
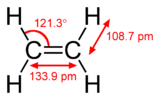
- Ethylén (C2H4): dvojná vazba obsahuje jednu σ‑vazbu a jednu π‑vazbu; π vzniká z bočního překrytí dvou p‑orbitalů a zabraňuje rotaci, což umožňuje existenci cis/trans izomerů u substituovaných alkenů.
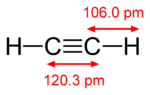
- Acetylén (C2H2): trojná vazba má jednu σ a dvě π vazby — π orbitaly jsou navzájem navzájem ortogonální (kolmé), takže existují dvě nezávislé π překrytí.
- Butadien a delokalizace: v 1,3‑butadienu je konjugace dvou π vazeb; elektrony jsou částečně delokalizované přes čtyři uhlíky, což snižuje energii systému a ovlivňuje reaktivitu (např. Diels–Alderovy reakce).
- Benzén: klasický příklad úplně delokalizovaného π systému (6 π elektronů) vedoucího k aromatické stabilitě.
Důsledky pro reaktivitu a strukturu
Protože π‑elektrony jsou relativně snadno dostupné, π‑systémy se často účastní:
- elektrofilních adičních reakcí (u alkenů),
- elektrofilních aromatických substitucí (u aromátů, kde místo adice dochází k substituci díky zachování aromatického systému),
- reakcí pericyklických (např. Diels–Alder), které využívají konjugované π systému.
Poznámka o d‑orbitalech a hypervalenci
U některých složitějších sloučenin nebo u prvků 3. periody se v historických interpretacích uvažovalo zapojení d‑orbitalů do π vazby. Moderní kvantově‑chemická analýza však často ukazuje, že vysvětlení hypervalentních struktur lépe zahrnují rezonanční formy a elektronovou delokalizaci než jednoduché „d‑π“ skládání. Nicméně u přechodných kovů a koordinační chemie hrají d‑orbitaly klíčovou roli v tvorbě π‑interakcí (např. zpětná π‑donace u karbonylů kovů).
Závěr
Vazby typu π jsou zásadní pro pochopení struktury, stability a reaktivity mnoha organických i anorganických sloučenin. Jsou méně silné než σ‑vazby, omezují rotaci kolem vazeb, mohou se delokalizovat v konjugovaných systémech a mají významné důsledky pro spektroskopii a syntézu organických sloučenin.