Enzym
Enzymy jsou bílkovinné molekuly v buňkách, které fungují jako biologické katalyzátory. Enzymy urychlují chemické reakce v těle, ale přitom se nevyčerpávají, a proto je lze používat znovu a znovu.
Téměř všechny biochemické reakce v živých organismech vyžadují enzymy. S enzymem probíhají chemické reakce mnohem rychleji než bez enzymu.p39 Dalšími biokatalyzátory jsou katalytické molekuly RNA, zvané ribozymy.
Látky na začátku reakce se nazývají substráty. Látky na konci reakce se nazývají produkty. Enzymy působí na substráty a mění je na produkty. Studium enzymů se nazývá enzymologie.
První enzym objevil v roce 1833 Anselme Payen.
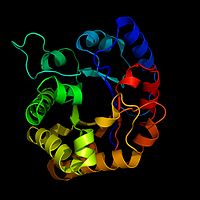
Páskový diagram enzymu zvaného TIM

Páskový diagram enzymu zvaného TIM
Struktura enzymu
Existují tisíce různých enzymů a každý z nich je specifický pro reakci, kterou katalyzuje. Enzymy mají názvy, které ukazují, co dělají. Názvy enzymů obvykle končí na -ase, což ukazuje, že se jedná o enzymy. Příkladem může být ATP syntáza. Vyrábí chemickou látku zvanou ATP. Dalším příkladem je DNA polymeráza. Čte neporušené vlákno DNA a používá ho jako předlohu k vytvoření nového vlákna.Příkladem enzymu je amyláza, která se nachází ve slinách. Rozkládá molekuly škrobu na menší molekuly glukózy a maltózy. Dalším druhem enzymu je lipáza. Rozkládá tuky na menší molekuly, mastné kyseliny a glycerol.d
Proteázy představují celou třídu enzymů. Rozkládají jiné enzymy a bílkoviny zpět na aminokyseliny. Nukleázy jsou enzymy, které řežou DNA nebo RNA, často na určitém místě v molekule.
Enzymy neslouží pouze k rozkladu velkých chemických látek na menší. Jiné enzymy přijímají menší chemické látky a vytvářejí z nich větší chemické látky a provádějí mnoho dalších chemických úkolů. Níže uvedená klasifikace uvádí hlavní typy.
Biochemici často kreslí obrázek enzymu, který slouží jako názorná pomůcka nebo mapa enzymu. To je obtížné, protože v enzymu mohou být stovky nebo tisíce atomů. Biochemici nemohou nakreslit všechny tyto detaily. Místo toho používají stuhové modely jako obrázky enzymů. Stužkové modely mohou zobrazit tvar enzymu, aniž by bylo nutné kreslit každý atom.
Většina enzymů nefunguje, pokud není správná teplota a pH. U savců je správná teplota obvykle přibližně 37o °C (tělesná teplota). Správné pH se může značně lišit. Pepsin je příkladem enzymu, který nejlépe funguje, když je pH přibližně 1,5.
Zahřátím enzymu nad určitou teplotu dojde k jeho trvalému zničení. Rozloží se proteázou a chemické látky se znovu použijí.
Některé chemické látky mohou pomoci enzymu vykonávat jeho práci ještě lépe. Tyto látky se nazývají aktivátory. Někdy může chemická látka enzym zpomalit nebo dokonce způsobit, že enzym nepracuje vůbec. Tyto látky se nazývají inhibitory. Většina léků jsou chemické látky, které buď urychlují, nebo zpomalují některý enzym v lidském těle.
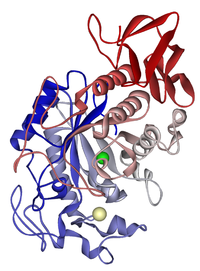
Salivární amyláza: chloridový iont zelený; vápník béžový
Struktura enzymu
Existují tisíce různých enzymů a každý z nich je specifický pro reakci, kterou katalyzuje. Enzymy mají názvy, které ukazují, co dělají. Názvy enzymů obvykle končí na -ase, což ukazuje, že se jedná o enzymy. Příkladem může být ATP syntáza. Vyrábí chemickou látku zvanou ATP. Dalším příkladem je DNA polymeráza. Čte neporušené vlákno DNA a používá ho jako předlohu k vytvoření nového vlákna.Příkladem enzymu je amyláza, která se nachází ve slinách. Rozkládá molekuly škrobu na menší molekuly glukózy a maltózy. Dalším druhem enzymu je lipáza. Rozkládá tuky na menší molekuly, mastné kyseliny a glycerol.d
Proteázy představují celou třídu enzymů. Rozkládají jiné enzymy a bílkoviny zpět na aminokyseliny. Nukleázy jsou enzymy, které řežou DNA nebo RNA, často na určitém místě v molekule.
Enzymy neslouží pouze k rozkladu velkých chemických látek na menší. Jiné enzymy přijímají menší chemické látky a vytvářejí z nich větší chemické látky a provádějí mnoho dalších chemických úkolů. Níže uvedená klasifikace uvádí hlavní typy.
Biochemici často kreslí obrázek enzymu, který slouží jako názorná pomůcka nebo mapa enzymu. To je obtížné, protože v enzymu mohou být stovky nebo tisíce atomů. Biochemici nemohou nakreslit všechny tyto detaily. Místo toho používají stuhové modely jako obrázky enzymů. Stužkové modely mohou zobrazit tvar enzymu, aniž by bylo nutné kreslit každý atom.
Většina enzymů nefunguje, pokud není správná teplota a pH. U savců je správná teplota obvykle přibližně 37o °C (tělesná teplota). Správné pH se může značně lišit. Pepsin je příkladem enzymu, který nejlépe funguje, když je pH přibližně 1,5.
Zahřátím enzymu nad určitou teplotu dojde k jeho trvalému zničení. Rozloží se proteázou a chemické látky se znovu použijí.
Některé chemické látky mohou pomoci enzymu vykonávat jeho práci ještě lépe. Tyto látky se nazývají aktivátory. Někdy může chemická látka enzym zpomalit nebo dokonce způsobit, že enzym nepracuje vůbec. Tyto látky se nazývají inhibitory. Většina léků jsou chemické látky, které buď urychlují, nebo zpomalují některý enzym v lidském těle.

Salivární amyláza: chloridový iont zelený; vápník béžový
Model zámku a klíče
Enzymy jsou velmi specifické. V roce 1894 Emil Fischer navrhl, že enzym i substrát mají specifické komplementární geometrické tvary, které do sebe přesně zapadají. Tento model se často označuje jako "zámek a klíč". Tento model však nevysvětluje, co se děje dále.V roce 1958 navrhl Daniel Koshland modifikaci modelu zámku a klíče. Protože enzymy jsou poměrně flexibilní struktury, aktivní místo se přetváří interakcí se substrátem. V důsledku toho se substrát neváže jednoduše na rigidní aktivní místo. Postranní řetězce aminokyselin v aktivním místě jsou ohýbány do poloh, aby enzym vykonával svou katalytickou činnost. V některých případech, například u glykosidáz, mění molekula substrátu při vstupu do aktivního místa také mírně svůj tvar.
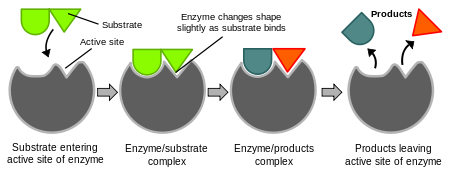
Diagramy znázorňující hypotézu o indukovaném přizpůsobení účinku enzymů
Model zámku a klíče
Enzymy jsou velmi specifické. V roce 1894 Emil Fischer navrhl, že enzym i substrát mají specifické komplementární geometrické tvary, které do sebe přesně zapadají. Tento model se často označuje jako "zámek a klíč". Tento model však nevysvětluje, co se děje dále.V roce 1958 navrhl Daniel Koshland modifikaci modelu zámku a klíče. Protože enzymy jsou poměrně flexibilní struktury, aktivní místo se přetváří interakcí se substrátem. V důsledku toho se substrát neváže jednoduše na rigidní aktivní místo. Postranní řetězce aminokyselin v aktivním místě jsou ohýbány do poloh, aby enzym vykonával svou katalytickou činnost. V některých případech, například u glykosidáz, mění molekula substrátu při vstupu do aktivního místa také mírně svůj tvar.

Diagramy znázorňující hypotézu o indukovaném přizpůsobení účinku enzymů
Funkce
Obecná rovnice pro enzymovou reakci je:
Substrát + enzym -> Substrát:enzym -> Produkt:enzym -> Produkt + enzym
Enzymy snižují aktivační energii reakce tím, že se substrátem vytvářejí intermediární komplex. Tento komplex se nazývá komplex enzym-substrát.
Například sacharáza, která je 400krát větší než její substrát sacharóza, štěpí sacharózu na její složky, kterými jsou glukóza a fruktóza. Sacharasa ohýbá sacharózu a napíná vazbu mezi glukózou a fruktózou. Molekuly vody se připojí a provedou štěpení ve zlomku sekundy. Enzymy mají tyto klíčové vlastnosti:
- Jsou katalytické. Běžně zvyšují rychlost reakce 10 miliardkrát.p39 Samotný enzym se reakcí nemění.
- Jsou účinné v malém množství. Jedna molekula enzymu může přeměnit 1000 molekul substrátu za minutu a o některých je známo, že jich za minutu přemění 3 miliony.p39
- Jsou velmi specifické. Jeden enzym provede pouze jednu z mnoha reakcí, kterých je substrát schopen.
Řízení aktivity enzymů
Aktivita enzymů je v buňce řízena pěti hlavními způsoby.
- Produkce enzymů (transkripce a translace enzymových genů) může být zvýšena nebo snížena v reakci na změny v prostředí buňky. Tato forma regulace genů se nazývá indukce a inhibice enzymů. Například u bakterií, které jsou rezistentní vůči antibiotikům, jako je penicilin, jsou indukovány enzymy, které hydrolyzují molekulu penicilinu.
- Enzymy se mohou vyskytovat v různých buněčných kompartmentech. Například mastné kyseliny jsou syntetizovány jednou sadou enzymů v cytosolu, endoplazmatickém retikulu a Golgiho aparátu. Poté jsou využity jinou sadou enzymů jako zdroj energie v mitochondriích.
- Enzymy mohou být regulovány svými vlastními produkty. Konečný produkt (produkty) například často inhibuje jeden z prvních enzymů dráhy. Takový regulační mechanismus se nazývá negativní zpětná vazba, protože množství produkovaného konečného produktu je regulováno jeho vlastní koncentrací. To zabraňuje tomu, aby buňky vytvářely příliš mnoho enzymu. Řízení činnosti enzymů pomáhá udržovat stabilní vnitřní prostředí v živých organismech.
- Enzymy lze regulovat tím, že se po výrobě upraví. Příkladem je štěpení polypeptidového řetězce. Chymotrypsin, trávicí proteáza, se vyrábí v neaktivní formě ve slinivce břišní a v této formě je transportován do žaludku, kde je aktivován. Tím se zabrání tomu, aby enzym trávil slinivku břišní nebo jiné tkáně dříve, než se dostane do střeva. Tento typ neaktivního prekurzoru enzymu se nazývá zymogen.
- Některé enzymy se mohou aktivovat při přechodu do jiného prostředí (např. z vysokého pH do nízkého pH). Například hemaglutinin v chřipkovém viru se aktivuje změnou tvaru. To je způsobeno kyselými podmínkami, které nastávají uvnitř lyzozomu hostitelské buňky.
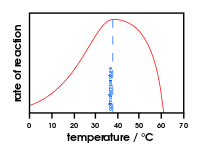
Graf znázorňující vliv změny teploty na aktivitu enzymu
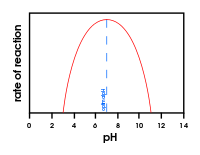
Graf znázorňující vliv změny pH na aktivitu enzymu
Funkce
Obecná rovnice pro enzymovou reakci je:
Substrát + enzym -> Substrát:enzym -> Produkt:enzym -> Produkt + enzym
Enzymy snižují aktivační energii reakce tím, že se substrátem vytvářejí intermediární komplex. Tento komplex se nazývá komplex enzym-substrát.
Například sacharáza, která je 400krát větší než její substrát sacharóza, štěpí sacharózu na její složky, kterými jsou glukóza a fruktóza. Sacharasa ohýbá sacharózu a napíná vazbu mezi glukózou a fruktózou. Molekuly vody se připojí a provedou štěpení ve zlomku sekundy. Enzymy mají tyto klíčové vlastnosti:
- Jsou katalytické. Běžně zvyšují rychlost reakce 10 miliardkrát.p39 Samotný enzym se reakcí nemění.
- Jsou účinné v malém množství. Jedna molekula enzymu může přeměnit 1000 molekul substrátu za minutu a o některých je známo, že jich za minutu přemění 3 miliony.p39
- Jsou velmi specifické. Jeden enzym provede pouze jednu z mnoha reakcí, kterých je substrát schopen.
Řízení aktivity enzymů
Aktivita enzymů je v buňce řízena pěti hlavními způsoby.
- Produkce enzymů (transkripce a translace enzymových genů) může být zvýšena nebo snížena v reakci na změny v prostředí buňky. Tato forma regulace genů se nazývá indukce a inhibice enzymů. Například u bakterií, které jsou rezistentní vůči antibiotikům, jako je penicilin, jsou indukovány enzymy, které hydrolyzují molekulu penicilinu.
- Enzymy se mohou vyskytovat v různých buněčných kompartmentech. Například mastné kyseliny jsou syntetizovány jednou sadou enzymů v cytosolu, endoplazmatickém retikulu a Golgiho aparátu. Poté jsou využity jinou sadou enzymů jako zdroj energie v mitochondriích.
- Enzymy mohou být regulovány svými vlastními produkty. Konečný produkt (produkty) například často inhibuje jeden z prvních enzymů dráhy. Takový regulační mechanismus se nazývá negativní zpětná vazba, protože množství produkovaného konečného produktu je regulováno jeho vlastní koncentrací. To zabraňuje tomu, aby buňky vytvářely příliš mnoho enzymu. Řízení činnosti enzymů pomáhá udržovat stabilní vnitřní prostředí v živých organismech.
- Enzymy lze regulovat tím, že se po výrobě upraví. Příkladem je štěpení polypeptidového řetězce. Chymotrypsin, trávicí proteáza, se vyrábí v neaktivní formě ve slinivce břišní a v této formě je transportován do žaludku, kde je aktivován. Tím se zabrání tomu, aby enzym trávil slinivku břišní nebo jiné tkáně dříve, než se dostane do střeva. Tento typ neaktivního prekurzoru enzymu se nazývá zymogen.
- Některé enzymy se mohou aktivovat při přechodu do jiného prostředí (např. z vysokého pH do nízkého pH). Například hemaglutinin v chřipkovém viru se aktivuje změnou tvaru. To je způsobeno kyselými podmínkami, které nastávají uvnitř lyzozomu hostitelské buňky.

Graf znázorňující vliv změny teploty na aktivitu enzymu

Graf znázorňující vliv změny pH na aktivitu enzymu
Inhibitory enzymů
Inhibitory lze použít k zastavení vazby enzymu na substrát. To může být provedeno za účelem zpomalení reakce řízené enzymem. Inhibitory zapadají volně nebo částečně do aktivního místa enzymu. Tím se zabrání nebo zpomalí tvorba komplexu enzym-substrát.
Inhibitory enzymů
Inhibitory lze použít k zastavení vazby enzymu na substrát. To může být provedeno za účelem zpomalení reakce řízené enzymem. Inhibitory zapadají volně nebo částečně do aktivního místa enzymu. Tím se zabrání nebo zpomalí tvorba komplexu enzym-substrát.
Denaturace
Denaturace je nevratná změna aktivního místa enzymu způsobená extrémní změnou teploty nebo pH. Sníží rychlost reakce, protože molekula substrátu se nevejde do aktivního místa, takže produkty nemohou vznikat.
Denaturace
Denaturace je nevratná změna aktivního místa enzymu způsobená extrémní změnou teploty nebo pH. Sníží rychlost reakce, protože molekula substrátu se nevejde do aktivního místa, takže produkty nemohou vznikat.
Kofaktory
Kofaktory neboli koenzymy jsou pomocné molekuly, které jsou potřebné pro fungování enzymu. Nejsou to bílkoviny a mohou to být organické nebo anorganické molekuly. Oba typy molekul někdy obsahují ve svém středu ion kovu, například klastry Mg2+, Cu2+, Mn 2+nebo železa a síry. Je to proto, že tyto ionty mohou působit jako donory elektronů, což je důležité v mnoha reakcích. Potřeba různých malých pomocníků enzymů je základním důvodem, proč živočichové včetně nás potřebují stopové prvky a vitaminy.
Kofaktory
Kofaktory neboli koenzymy jsou pomocné molekuly, které jsou potřebné pro fungování enzymu. Nejsou to bílkoviny a mohou to být organické nebo anorganické molekuly. Oba typy molekul někdy obsahují ve svém středu ion kovu, například klastry Mg2+, Cu2+, Mn 2+nebo železa a síry. Je to proto, že tyto ionty mohou působit jako donory elektronů, což je důležité v mnoha reakcích. Potřeba různých malých pomocníků enzymů je základním důvodem, proč živočichové včetně nás potřebují stopové prvky a vitaminy.
Klasifikace
Enzymy byly klasifikovány Mezinárodní biochemickou unií. Její Komise pro enzymy rozdělila všechny známé enzymy do šesti tříd:
- Oxido-reduktázy: katalyzují přenos elektronů
- Transferázy: přesun funkční skupiny z jedné molekuly na druhou
- Hydrolázy: přidávají -OH (hydroxylovou) skupinu
- Lyázy: štěpí chemické vazby a často přidávají dvojnou vazbu nebo kruhovou strukturu.
- Izomerázy: A -> B, kde B je izomer A
- Ligázy: spojují dvě velké molekuly: Ab + C -> A-C + b
Jednotlivým enzymům je přiřazeno čtyřmístné číslo, které je v databázi klasifikuje. p145
Klasifikace
Enzymy byly klasifikovány Mezinárodní biochemickou unií. Její Komise pro enzymy rozdělila všechny známé enzymy do šesti tříd:
- Oxido-reduktázy: katalyzují přenos elektronů
- Transferázy: přesun funkční skupiny z jedné molekuly na druhou
- Hydrolázy: přidávají -OH (hydroxylovou) skupinu
- Lyázy: štěpí chemické vazby a často přidávají dvojnou vazbu nebo kruhovou strukturu.
- Izomerázy: A -> B, kde B je izomer A
- Ligázy: spojují dvě velké molekuly: Ab + C -> A-C + b
Jednotlivým enzymům je přiřazeno čtyřmístné číslo, které je v databázi klasifikuje. p145
Použití enzymů
Enzymy se komerčně používají k:
- výroba kojenecké stravy - předtrávená strava pro kojence
- změkčování středů čokolád
- biologický prací prášek - obsahuje enzymy proteázy, které rozkládají špínu a nečistoty. Rozkládá velké, nerozpustné molekuly na malé, rozpustné molekuly. Pracuje při nižší teplotě, takže je zapotřebí méně energie (termostabilní).
Použití enzymů
Enzymy se komerčně používají k:
- výroba kojenecké stravy - předtrávená strava pro kojence
- změkčování středů čokolád
- biologický prací prášek - obsahuje enzymy proteázy, které rozkládají špínu a nečistoty. Rozkládá velké, nerozpustné molekuly na malé, rozpustné molekuly. Pracuje při nižší teplotě, takže je zapotřebí méně energie (termostabilní).
Související stránky
- Kinetika výbuchu
Související stránky
- Kinetika výbuchu
Otázky a odpovědi
Otázka: Co je to enzym?
Odpověď: Enzym je bílkovinná molekula v buňkách, která funguje jako biologický katalyzátor.
Otázka: Jakou funkci mají enzymy v těle?
Odpověď: Enzymy urychlují chemické reakce v těle, ale přitom se nevyčerpávají, takže je lze používat znovu a znovu.
Otázka: Potřebují všechny biochemické reakce v živých organismech enzymy?
Odpověď: Ano, téměř všechny biochemické reakce v živých organismech potřebují enzymy.
Otázka: Co jsou to substráty?
Odpověď: Substráty jsou látky na začátku reakce.
Otázka: Co jsou produkty?
Odpověď: Produkty jsou látky na konci reakce.
Otázka: Jak se nazývá studium enzymů?
Odpověď: Studium enzymů se nazývá enzymologie.
Otázka: Kdo objevil první enzym?
Odpověď: První enzym objevil v roce 1833 Anselme Payen.
Vyhledávání