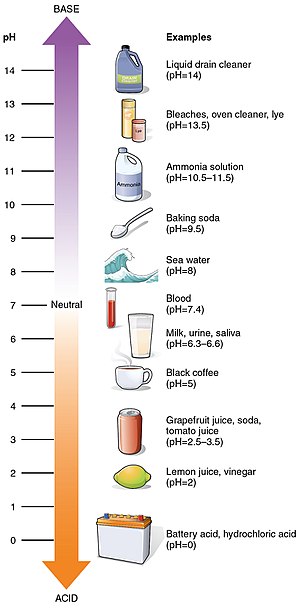
pH je stupnice kyselosti od 0 do 14. Udává, jak kyselá nebo zásaditá je látka. Kyselější roztoky mají nižší pH. Zásaditější roztoky mají vyšší pH. Látky, které nejsou kyselé ani zásadité (tj. neutrální roztoky), mají obvykle pH 7. Kyseliny mají pH nižší než 7. V případě kyselých roztoků je pH nižší. Zásady mají pH vyšší než 7.
pH je měřítkem koncentrace protonů (H+) v roztoku. Tento pojem zavedl S.P.L. Sørensen v roce 1909. Písmeno p znamená německy potenz, což znamená síla nebo koncentrace, a písmeno H znamená vodíkový ion (H+).
Nejběžnější vzorec pro výpočet pH je:
pH = - log 10 [ H + ] {\displaystyle {\mbox{pH}}=-\log _{10}\left[{\mbox{H}}^{+}\right]} ![{\displaystyle {\mbox{pH}}=-\log _{10}\left[{\mbox{H}}^{+}\right]}](https://www.alegsaonline.com/image/093977a79b6a17e02db4699475930e48c05d6468.svg)
[H+] označuje koncentraci iontů H+ (také se píše [H3O+], stejná koncentrace hydroniových iontů), měřeno v molech na litr (také známé jako molarita).
Správná rovnice však ve skutečnosti zní:
pH = - log 10 [ a H + ] {\displaystyle {\mbox{pH}}=-\log _{10}\left[a_{\mathrm {H^{+}} }\right]} ![{\displaystyle {\mbox{pH}}=-\log _{10}\left[a_{\mathrm {H^{+}} }\right]}](https://www.alegsaonline.com/image/7a631c4037415f3d4483a6cb07e69858b64890fc.svg)
kde a H + {\displaystyle a_{\mathrm {H^{+}} }}  označuje aktivitu iontů H+. Tato rovnice však ve většině případů poskytuje stejnou hodnotu jako běžnější vzorec, takže v úvodní chemii se jako definice pH uvádí předchozí rovnice.
označuje aktivitu iontů H+. Tato rovnice však ve většině případů poskytuje stejnou hodnotu jako běžnější vzorec, takže v úvodní chemii se jako definice pH uvádí předchozí rovnice.
Většina látek má pH v rozmezí 0 až 14, avšak extrémně kyselé nebo zásadité látky mohou mít pH < 0 nebo pH > 14.
Alkalické látky mají místo vodíkových iontů koncentraci hydroxidových iontů (OH-).
Otázky a odpovědi
Otázka: Co je to pH?
Odpověď: pH je stupnice kyselosti od 0 do 14, která měří koncentraci protonů (H+) v roztoku. Udává, jak kyselá nebo zásaditá je látka, přičemž kyselejší roztoky mají nižší pH a zásaditější roztoky mají vyšší pH. Neutrální roztoky mají obvykle pH 7.
Otázka: Kdo zavedl pojem pH?
Odpověď: Tento pojem zavedl v roce 1909 S. P. L. Sørensen.
Otázka: Co znamená písmeno "p" ve slově "pH"?
Odpověď: Písmeno "p" znamená německé slovo potenz, což znamená síla nebo koncentrace.
Otázka: Jak se vypočítá pH?
Odpověď: Nejběžnější vzorec pro výpočet pH je záporný logaritmus desetinásobku koncentrace H+ iontů (také psáno [H3O+], což označuje stejnou koncentraci hydroniových iontů) měřených v molech na litr (nebo molarita). Existuje však také rovnice, která zohledňuje aktivitu namísto pouhé koncentrace a která může v závislosti na situaci poskytovat jiné hodnoty než běžnější vzorec.
Otázka: Jaký rozsah má většina látek na stupnici pH?
Odpověď: Většina látek má pH v rozmezí 0 až 14, i když extrémně kyselé nebo zásadité látky mohou mít hodnotu mimo tento rozsah (menší než 0 nebo větší než 14).
Otázka: Jak se na stupnici pH liší zásadité látky od kyselých? Odpověď: Alkalické látky mají na stupnici vyšší hodnoty díky koncentraci hydroxidových iontů (OH-) namísto vodíkových iontů jako kyseliny.

![{\displaystyle {\mbox{pH}}=-\log _{10}\left[{\mbox{H}}^{+}\right]}](https://www.alegsaonline.com/image/093977a79b6a17e02db4699475930e48c05d6468.svg)
![{\displaystyle {\mbox{pH}}=-\log _{10}\left[a_{\mathrm {H^{+}} }\right]}](https://www.alegsaonline.com/image/7a631c4037415f3d4483a6cb07e69858b64890fc.svg)