Sigmatropní reakce v organické chemii je pericyklická reakce. Sigmatropická reakce nevyužívá katalyzátor a zahrnuje jedinou molekulu (nekatalyzovaný intramolekulární proces). Mění jednu vazbu σ na jinou vazbu σ. Název sigmatropická vznikl složením dlouho zavedeného názvu "sigma" pro vazby mezi jednotlivými uhlíky a řeckým slovem tropos, což znamená obrat. Jedná se o reakci přeskupení, což znamená, že se vazby v molekule přesouvají mezi atomy, aniž by z molekuly nějaké atomy odešly nebo do ní přibyly nové. Při sigmatropní reakci se substituent přesouvá z jedné části systému s vazbou π do druhé části v rámci intramolekulární reakce za současného přeskupení systému π. Při sigmatropní reakci se substituent přesouvá z jedné části systému s vazbou π do druhé části. Skutečné sigmatropické reakce obvykle nepotřebují katalyzátor. Některé sigmatropické reakce jsou katalyzovány Lewisovou kyselinou. Sigmatropní reakce mají často katalyzátory z přechodných kovů, které tvoří meziprodukty v analogických reakcích. Nejznámější ze sigmatropických přeskupení jsou [3,3] Copeho přeskupení, Claisenovo přeskupení, Carrollovo přeskupení a Fischerova indolová syntéza.
Sigmatropická reakce
Přehled sigmatropických posunů
Woodward-Hoffmanova nomenklatura sigmatropického posunu
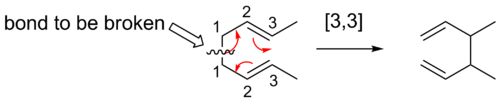
Pro popis sigmatropických posunů se používá speciální notace. Každému atomu uhlíku na páteři molekuly je přiřazeno číslo polohy. Sigmatropické přeskupení se popisuje pomocí pořadového členu [i,j]. To znamená migraci vazby σ sousedící s jedním nebo více systémy π do nové polohy (i-1) a (j-1) atomů vzdálených od původního umístění vazby σ. Pokud je součet i a j sudé číslo, znamená to zapojení neutrálního řetězce se všemi atomy C. Liché číslo naznačuje, že je přítomen nabitý atom C nebo osamělý pár heteroatomů nahrazující dvojnou vazbu uhlík-uhlík. Z posunů [1,5] a [3,3] se tak stávají posuny [1,4] a [2,3] s heteroatomy při zachování symetrie. Ve třetím příkladu jsou pro přehlednost vynechány vodíky.

Zde je způsob, jak zjistit pořadí daného sigmatropického uspořádání. Prvním krokem je přidělení čísel jednotlivým atomům, počínaje atomy přerušované vazby jako atom 1. Chemici počítají atomy v každém směru od přerušované vazby k atomům, které tvoří novou σ-vazbu v produktu. Čísla, která odpovídají atomům tvořícím novou vazbu, se pak oddělí čárkou a umístí do závorek. Tím vznikne deskriptor sigmatropické reakce.
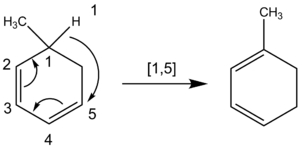
Chemici také počítají atomy při pojmenování sigmatropického posunu, při kterém se pohybuje atom vodíku. Při migraci atomu vodíku se řetězec uhlíku nepřerušuje. Chemici tedy počítají napříč všemi atomy, které se reakce účastní, a nikoli pouze napříč nejbližšími atomy. Například následující migrace atomu vodíku má pořadí [1,5], kterého se dosáhne počítáním proti směru hodinových ručiček přes systém π, a nikoli pořadí [1,3] přes kruhovou 2skupinu CH, které by chybně vzniklo při počítání ve směru hodinových ručiček.
Suprafaciální a antarafaciální posuny
Chemici studovali sigmatropní reakce, při nichž má migrující skupina sterocentrum. V zásadě mohou všechny sigmatropické posuny probíhat buď se stejnou (retenční), nebo opačnou (inverzní) geometrií migrující skupiny. To závisí na tom, zda se k vytvoření nové vazby použije původní vazebný lalok migrujícího atomu nebo jeho jiný lalok.
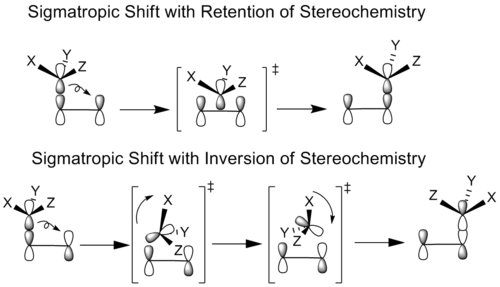
V případě stereochemické retence se migrující skupina přemístí bez rotace do vazebné polohy. V případě stereochemické inverze migrující skupina rotuje i translatuje, aby dosáhla vazebné konformace.
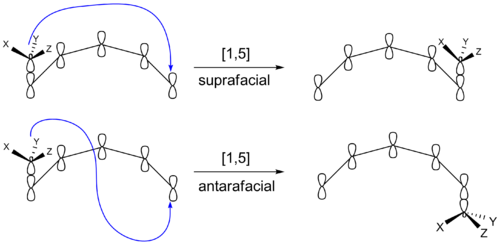
Existuje ještě jeden způsob, jak může sigmatropická reakce vést k produktům s odlišným sterochemickým složením. Migrující skupina může po rebondingu zůstat na původní straně π systému. Nebo může přejít na opačnou stranu systému π. Pokud migrující skupina zůstane na stejné straně systému π, je posun znám jako suprafaciální. Pokud migrující skupina přechází na opačnou stranu, nazývá se antarafaciální posun. Přeměny, ke kterým dochází v rámci malých nebo středně velkých kruhů, nemohou provádět antarafaciální posuny.
Třídy sigmatropických přeskupení
[1,3] Směny
Tepelné posuny hydridů
Při tepelném [1,3] hydridovém posunu se hydrid posune o tři atomy. Podle Woodwardových-Hoffmannových pravidel by měl probíhat antarafaciální posun. Ačkoli je takový posun symetricky přípustný, Möbiova topologie požadovaná v přechodovém stavu takový posun zakazuje. Je to geometricky nemožné. To je důvod, proč enoly neizomerizují bez kyselého nebo zásaditého katalyzátoru.
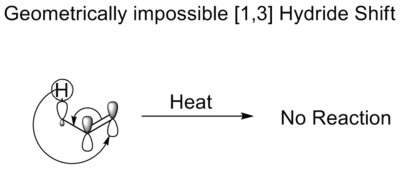
Tepelné alkylové posuny
Tepelné posuny alkyl [1,3], podobně jako posuny [1,3] hydridů, musí probíhat antarafaciálně. Geometrie přechodového stavu je prohibitivní. Alkylová skupina však může vzhledem k povaze svých orbitalů invertovat svou geometrii a vytvořit novou vazbu se zadním lalokem svého sp 3orbitalu. Výsledkem této reakce bude nadfázový posun. Tyto reakce zatím nejsou v systémech s otevřeným řetězcem běžné kvůli vysoce uspořádané povaze přechodového stavu. Reakce tedy lépe fungují v cyklických molekulách.
![[1,3] Alkyl Shifts](https://www.alegsaonline.com/image/550px-1,3alkylfixed.png)
Fotochemické [1,3] posuny
Fotochemické [1,3] posuny by měly být nadfázové, většina z nich je však nekonzistentní, protože probíhají přes tripletový stav (tj. mají diradikálový mechanismus, na který se Woodwardova-Hoffmannova pravidla nevztahují).
[1,5] Směny
Posun [1,5] zahrnuje posun 1 substituentu (-H, -R nebo -Ar) o 5 atomů systému π. Bylo prokázáno, že vodík se posouvá v cyklických systémech i systémech s otevřeným řetězcem při teplotách 200 ˚C nebo vyšších. Předpokládá se, že tyto reakce probíhají suprafaciálně, za pomoci přechodového stavu podle Huckelovy topologie.
![[1,5] Hydride shift in a cyclic system](https://www.alegsaonline.com/image/300px-1,5hydridecyclicfixed.png)
Fotoozáření by vyžadovalo antarafaciální posun vodíku. Ačkoli jsou takové reakce vzácné, existují příklady, kdy je antarafaciální posun upřednostňován:
![Antarafacial [1,5] Hydride Shift](https://www.alegsaonline.com/image/600px-1,5hantarafacialfixed.png)
Na rozdíl od vodíkových [1,5] posunů nebyly nikdy pozorovány žádné [1,5] alky posuny v systému s otevřeným řetězcem. Chemici určili rychlostní preference pro [1,5] alkylové posuny v cyklických systémech: karbonyl a karboxyl> hydrid> fenyl a vinyl>> alkyl.
Alkylové skupiny podléhají [1,5] posunu velmi špatně a obvykle vyžadují vysoké teploty. U cyklohexadienů však teplota pro alkylové posuny není o mnoho vyšší než u karbonylů, které jsou nejlépe migrující skupinou. Studie ukázala, že je to proto, že alkylové posuny na cyklohexadienu probíhají jiným mechanismem. Nejprve se kruh otevře, následuje [1,7] posun a poté se kruh elektrocyklicky reformuje:
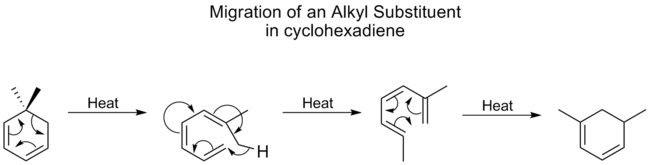
Stejný mechanistický proces, bez závěrečné elektrocyklické reakce uzavírání kruhu, je vidět níže při přeměně lumisterolu na vitamin D2.
[1,7] Směny
[1,7] sigmatropické posuny jsou podle Woodwardových-Hoffmannových pravidel předpovězeny jako antarafaciální, tedy jako přechodový stav Möbiovy topologie. Antarafaciální [1,7] posun je pozorován při přeměně lumisterolu na vitamin D 2, kde po elektrocyklickém otevření kruhu na previtamin D dochází k 2posunu methylového vodíku.
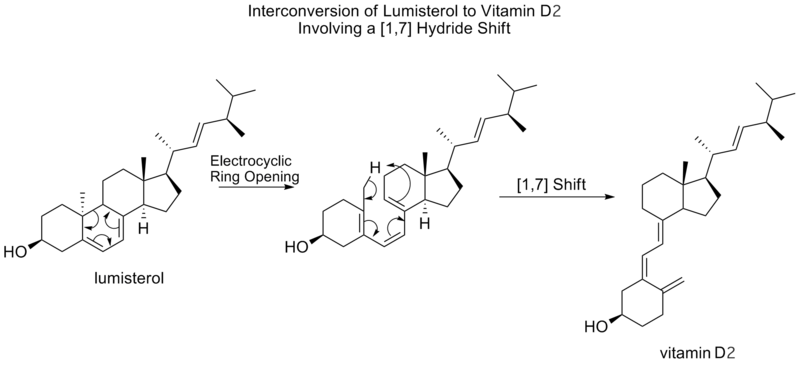
Bicyklické nonatrieny také podléhají [1,7] posunům v rámci tzv. walk rearrangement, což je posun dvojmocné skupiny jako součásti tříčlenného kruhu v bicyklické molekule.
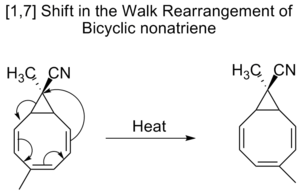
[3,3] Směny
[3,3] sigmatropické posuny jsou dobře prostudované sigmatropické přestavby. Woodwardova-Hoffmanova pravidla předpovídají, že tyto šestielektronové reakce budou probíhat suprafaciálně za použití přechodového stavu s Huckelovou topologií.
Claisenovo přeuspořádání
Claisenova přestavba, kterou v roce 1912 objevil Rainer Ludwig Claisen, je prvním zaznamenaným příkladem [3,3]-sigmatropické přestavby. Tato přestavba je užitečnou reakcí, při níž se vytváří vazba uhlík-uhlík. Příkladem Claisenovy přestavby je [3,3] přestavba allylovinyletheru, při níž po zahřátí vzniká γ,δ-nenasycený karbonyl. Vznik karbonylové skupiny způsobuje, že tato reakce je na rozdíl od jiných sigmatropických přeskupení ze své podstaty nevratná.

Aromatická Claisenova přestavba
Orto-Claisenova přestavba zahrnuje [3,3] posun allylfenyletheru na meziprodukt, který rychle tautomerizuje na orto-substituovaný fenol.
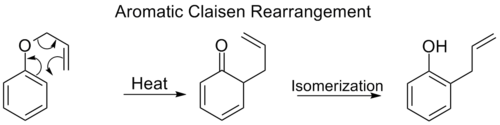
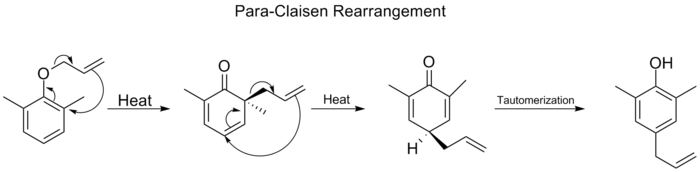
Pokud jsou obě ortho polohy na benzenovém kruhu blokovány, dojde k druhé orto-klaisenové přestavbě. Tato para-Claisenova přestavba končí tautomerizací na tri-substituovaný fenol.
Přeuspořádání Cope
Copeova přestavba je rozsáhle studovaná organická reakce zahrnující [3,3] sigmatropickou přestavbu 1,5-dienů. Vyvinul ji Arthur C. Cope. Například 3,4-dimethyl-1,5hexadien zahřátý na 300 °C poskytuje 2,6-oktadien.

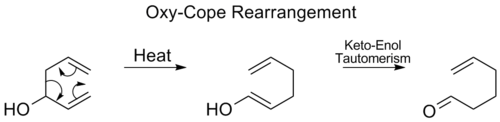
Přeskupení Oxy-Cope
Oxy-Cope přeskupení hydroxylová skupina se přidává na C3 za vzniku enalu nebo enonu po keto-enolové tautomerii meziproduktu enolu:
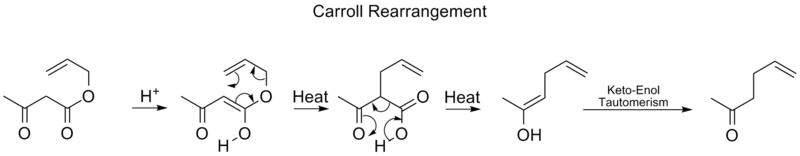
Carroll Rearrangement
Carrollova přestavba je přestavbová reakce v organické chemii a zahrnuje přeměnu β-keto-allylesteru na α-allyl-β-ketokarboxylovou kyselinu. Po této organické reakci může následovat dekarboxylace a konečným produktem je γ,δ-allylketon. Carrollova přestavba je adaptací Claisenovy přestavby a účinně se jedná o dekarboxylační allylaci.
Fischerova syntéza indolů
Fischerova indolová syntéza je chemická reakce, při níž se z (substituovaného) fenylhydrazinu a aldehydu nebo ketonu za kyselých podmínek získává aromatický heterocyklus indol. Reakci objevil v roce 1883 Hermann Emil Fischer.
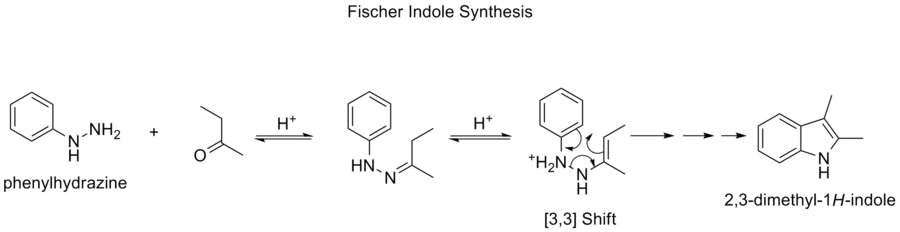
Volba kyselého katalyzátoru je velmi důležitá. Mezi úspěšné kyselé katalyzátory patří: Bronstedovy kyseliny, jako je HCl, H2SO4 , kyselina polyfosforečná a kyselina p-toluensulfonová. Užitečnými katalyzátory jsou také Lewisovy kyseliny, jako je trifluorid boru, chlorid zinečnatý, chlorid železitý a chlorid hlinitý.
Bylo publikováno několik recenzí.
[5,5] Směny
Podobně jako u posunů [3,3] Woodwardova-Hoffmanova pravidla předpovídají, že sigmatropické posuny [5,5] budou probíhat suprafaciálně, tedy ve stavu Huckelovy topologie přechodu. Tyto reakce jsou vzácnější než [3,3] sigmatropické posuny, ale to je dáno především tím, že molekuly, které mohou projít [5,5] posuny, jsou vzácnější než molekuly, které mohou projít [3,3] posuny.
![[5,5] shift of phenyl pentadienyl ether](https://www.alegsaonline.com/image/800px-5,5shiftfixeds.png)
Přeskupení procházek
Migrace dvojmocné skupiny, jako je O, S, NR nebo CR2 , která je součástí tříčlenného kruhu v bicyklické molekule, se běžně označuje jako walkova přestavba. Tu lze formálně charakterizovat podle Woodwardových-Hofmannových pravidel jako (1, n) sigmatropický posun. Příkladem takového přeskupení je posun substituentů na tropilidenech (1,3,5-cykloheptatrienech). Při zahřívání prochází pi-systém elektrocyklickým uzavíráním kruhu za vzniku bicyk[4,1,0]heptadienu (norkaradienu). Poté následuje [1,5] alkylový posun a elektrocyklické otevření kruhu.
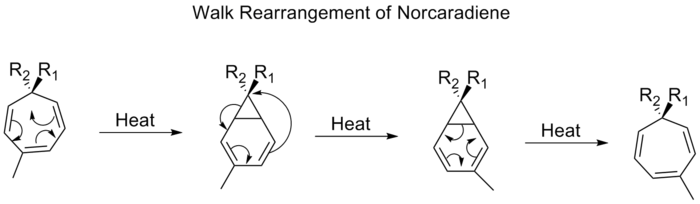
Očekává se, že Walkova přestavba norkaradienů, která probíhá prostřednictvím [1,5] posunu, bude probíhat suprafaciálně se zachováním stereochemie. Experimentální pozorování však ukazují, že 1,5 posun norkaradienů probíhá antarafaciálně. Teoretické výpočty zjistily, že [1,5] posun je diradikálový proces, ale bez účasti diradikálových minim na povrchu potenciální energie.
Související stránky
- 2,3-sigmatropní přestavba
- Změna NIH
- Teorie hraničních molekulových orbitalů
- Woodwardova-Hoffmannova pravidla
Otázky a odpovědi
Otázka: Co je to sigmatropní reakce v organické chemii?
Odpověď: Sigmatropní reakce je pericyklická reakce, která zahrnuje nekatalyzovaný intramolekulární proces a mění jednu σ-vazbu na jinou σ-vazbu.
Otázka: Zahrnuje sigmatropická reakce katalyzátor?
Odpověď: Skutečná sigmatropická reakce obvykle nezahrnuje katalyzátor, i když některé sigmatropické reakce mohou být katalyzovány Lewisovou kyselinou.
Otázka: Co znamená termín "sigmatropická"?
Odpověď: Termín "sigmatropický" je složené slovo složené ze slova "sigma", které označuje vazby mezi jednotlivými uhlíky, a řeckého slova "tropos", které znamená obrat.
Otázka: Jaký druh reakce je sigmatropická reakce?
Odpověď: Sigmatropická reakce je reakce přeskupení, což znamená, že se vazby v molekule mezi atomy přesouvají, aniž by se atomy z molekuly vytrácely nebo se do ní přidávaly nové atomy.
Otázka: Co se děje při intramolekulární sigmatropické reakci?
Odpověď: Při intramolekulární sigmatropické reakci se substituent přesouvá z jedné části systému s vazbou π do druhé části za současného přeskupení systému π.
Otázka: Existují nějaké známé sigmatropické přestavby?
Odpověď: Mezi nejznámější sigmatropické přestavby patří [3,3] Copeova přestavba, Claisenova přestavba, Carrollova přestavba a Fischerova syntéza indolu.
Otázka: Zahrnují sigmatropické reakce často katalyzátory z přechodných kovů?
Odpověď: Ano, sigmatropické reakce mají často katalyzátory z přechodných kovů, které tvoří meziprodukty v analogických reakcích.