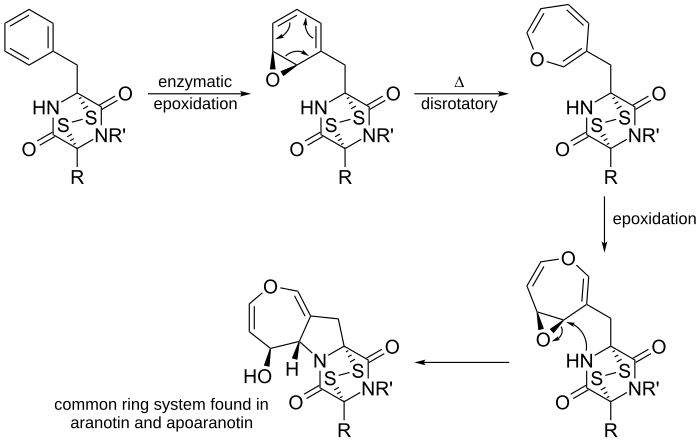
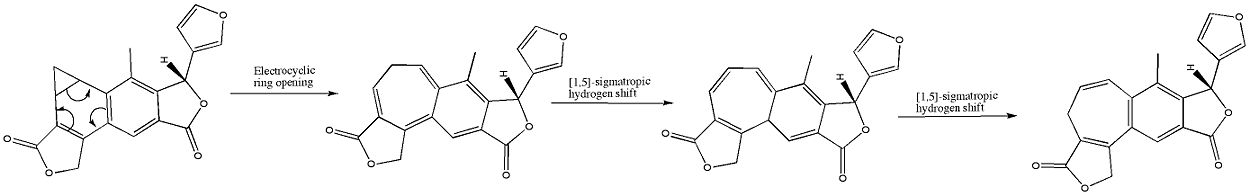
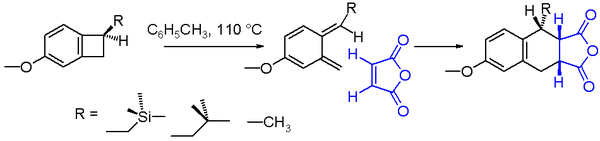
V organické chemii je elektrocyklická reakce typem pericyklické přeskupovací reakce, při které se mění počet a uspořádání vazeb mezi soustavou konjugovaných π-elektronů a jednou σ-vazbou. Reakce je elektrocyklická tehdy, když se v jejím důsledku z jedné vazby pí vytvoří jedna vazba sigma (uzavření kruhu, tzv. elektrocyklizace) nebo naopak vznikne z jedné σ-vazby nová vazba π (otevření kruhu). Tyto reakce jsou charakteristické tím, že probíhají přes uspořádaný, cyklický přechodový stav, v němž dochází k simultánnímu přesunu elektronů.
- elektrocyklické reakce mohou být fotoindukované) nebo tepelné (tepelně iniciované), přičemž způsob aktivace často mění stereochemický výsledek;
- způsob reakce je určen počtem π-elektronů v konjugované části (tj. systém odpovídá buď 4n nebo 4n+2 π-elektronům) a podle toho platí pravidla typu Woodward–Hoffmann;
- elektrocyklická reakce může uzavřít kruh (elektrocyklizace) nebo otevřít kruh a převést cyklický substrát na konjugovaný diolefin;
- stereospecifita výsledku je určena konrotatorním nebo disrotatorním průběhem přechodového stavu, jak předpovídají Woodwardova-Hoffmannova pravidla;
- výsledek (tj. konfigurace produktů) lze často vysvětlit pomocí hraničně-orbitální metody (FMO), která sleduje fáze HOMO/LUMO.
Woodward–Hoffmannova pravidla a elektronové počty
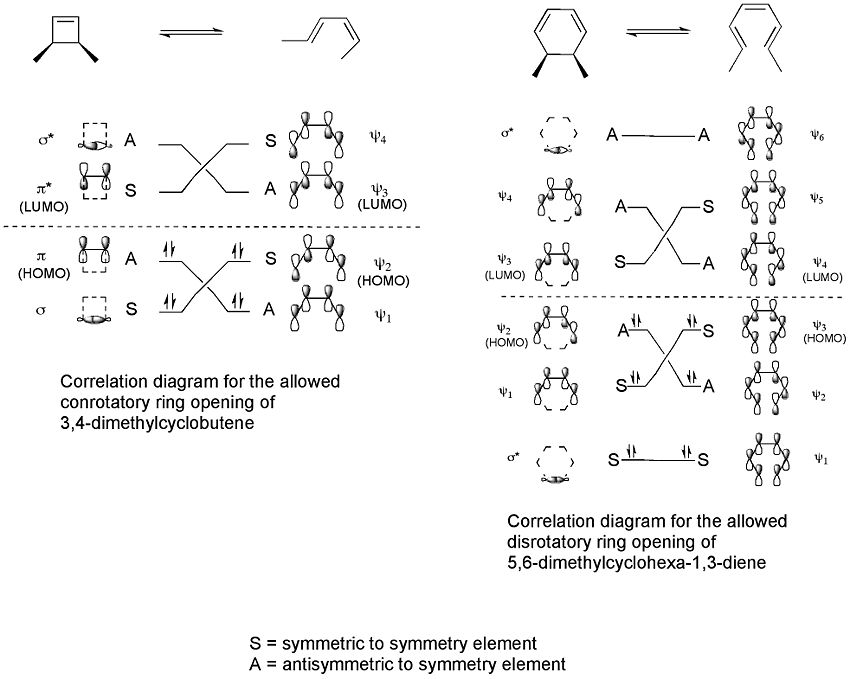
Klíčovým vodítkem pro předpověď stereochemie elektrocyklických reakcí jsou Woodwardova-Hoffmannova pravidla, která vycházejí ze zachování symetrie molekulových orbitalů. Pro elektrocyklizaci platí zjednodušeně:
- termálně: pro systémy s (4n) π-elektrony probíhá reakce konrotatorně; pro systémy s (4n+2) π-elektrony probíhá disrotatorně;
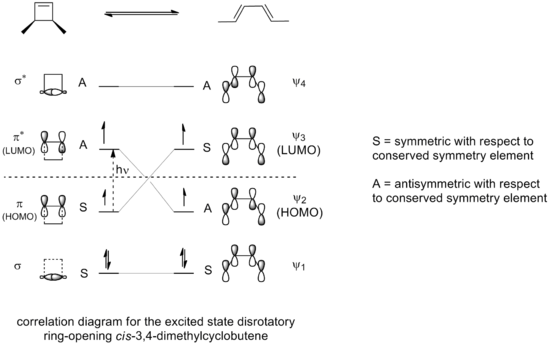
- fotochemicky: pořadí se obrací — (4n) π-elektronové systémy preferují disrotaci a (4n+2) π systémy konrotaci.
Tato pravidla vysvětlují, proč např. termální otevření cyklobutenu (4 π) probíhá konrotatorně (viz příklad níže), zatímco termální uzavření hexa-1,3,5-trienu na cyklohexadien probíhá disrotatorně (6 π, tedy 4n+2, n=1).
Hraničně-orbitální (FMO) vysvětlení
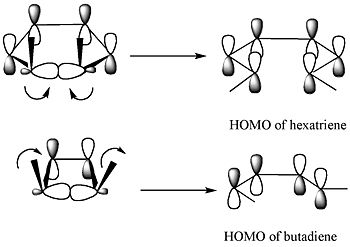
Metoda hraničních orbitalů sleduje symetrii a fáze nejvyšší obsazené molekulové orbitaly (HOMO) substrátu nebo produktu. Při elektrocyklické přeměně musí fázové relace orbitalů na koncích polyénu souhlasit tak, aby při jejich vzájemném překrytí nevznikala nové antivazba, což určuje, zda bude přednostně probíhat konrotace nebo disrotace. Pokud fáze laloků na koncích polyénu v HOMO odpovídají stejnému znaménku, uzavření bude vyžadovat pohyb, který tyto laloky spojí bez fázového rozporu.
Stereochemie, konrotace vs. disrotace a torkoselektivita
Stereospecifičnost elektrocyklických reakcí je přímým důsledkem směru, jakým se koncové atomy rotují během zavírání či otevírání. Termíny konrotatorní a disrotatorní popisují, zda se koncové skupiny otáčejí stejným směrem (konrotace) nebo opačnými směry (disrotace). Konkrétní stereochemický výsledek (cis/trans uspořádání, konfigurace substituentů) závisí na původní geometrii substrátu a na tom, který režim je symetrií povolen.
Torkoselektivita v elektrocyklické reakci se vztahuje ke směru, kterým se substituenty otáčejí. I v případě konrotatorní reakce, kde obecně existují dvě možné směry rotace (obě vedou k enantiomerním produktům), mohou sterické nebo elektronové efekty preferovat jednu rotaci nad druhou. To vede k preferenci jednoho enantiomeru (částečná nebo úplná torkvoselektivita). Prakticky se torkoselektivita uplatňuje při stereoselektivní syntéze, často ve spojení s chiralizujícími činidly nebo katalyzátory, které asymetricky polarizují přechodový stav.
Příklady a aplikace
Nazarovova cyklizace: Chemici často uvádějí Nazarovovu cyklizační reakci jako významnou elektrocyklickou přeměnu. Jedná se o uzavírání kruhu divinylketonů na cyklopentenony; mechanismus typicky zahrnuje aktivaci karbonylové skupiny Lewisovou nebo Brønstedovou kyselinou, generaci pentadienylového karbokationtu a následnou 4π-elektrocyklizaci (konrotatorní u termálně povolené verze). Reakce byla objevena Ivanem Nikolajevičem Nazarovem (1906–1957) a má široké využití v syntéze pětičlenných jader v přírodních produktech a léčivech. Moderní varianty zahrnují přerušované (interrupted) Nazarovovy cyklizace a enantioselektivní verze s chiralními katalyzátory.
Otevření 3,4-dimethylcyklobutenu (ilustrativní příklad): Příkladem termální elektrocyklické reakce je tepelné otevření kruhu 3,4-dimethylcyklobutenu. Z cis-izomeru vzniká pouze cis,trans-2,4-hexadien, zatímco z trans-izomeru vzniká trans,trans dien. Tento rozdíl vyplývá ze směru rotace koncových atomů během konrotatorního otevření kruhu (termální 4π systém → konrotace). Schéma ilustrující izomerizaci je na obrázku:
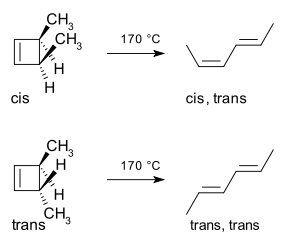
Hraničně-orbitální metoda vysvětluje tento průběh: σ-vazba, která se rozlomí při otevírání, poskytne laloky p-orbitálů s fázovým uspořádáním shodným s HOMO výsledného butadienu. K tomu dochází pouze při konrotativním otevření, které vede k opačným znaménkům pro oba laloky na přerušených koncích kruhu; disrotativní otevření by vytvořilo nevýhodné antivazebné překrytí. Schematické znázornění reakčního mechanismu je níže:
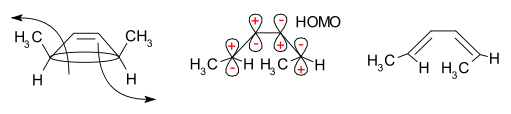
Praktické aspekty a měření stereochemie
V praxi chemici zjišťují stereochemii produktů pomocí NMR (NOE, coupling constants), chiralitních chromatografických metod (chiral HPLC), rotační dichroismu (CD) nebo krystalografie. Pro řízení stereochemie se často používají:
- sterické efekty substituentů, které preferují jeden směr rotace,
- elektronové efekty (donor/akceptor), které stabilizují určité přechodové stavy,
- katalytické systémy (Lewisovy kyseliny, organokatalýza, chiralní ligandy) umožňující enantioselektivitu nebo torkoselektivitu.
Závěr
Elektrocyklické reakce jsou základní třídu pericyklických procesů důležitých v syntetické organické chemii. Díky jednoduchým pravidlům založeným na počtu π-elektronů a zachování symetrie orbitalů lze spolehlivě předpovídat stereochemii produktů. Moderní výzkum pokračuje v rozvoji katalytických a enantioselektivních variant (např. enantioselektivní Nazarovovy cyklizace nebo torkvoselektivní elektrocyklizace), které rozšiřují možnosti jejich aplikace při konstrukci složitých cyklických skeletů.