Přehled
Nukleofil je chemický činidlo, které dává k dispozici elektronový pár a vytváří novou chemickou vazbu s elektrofilním centrem. Jinými slovy jde o částici s electronovým nadbytkem, která se přitahuje k oblastem s částečným nebo plným kladným nábojem. V tradiční terminologii odpovídá nukleofil definici Lewisovy báze. Nukleofily mohou být neutrální molekuly i nabité částice, přičemž společným znakem je přítomnost volného páru elektronů nebo elektronové hustoty snadno dostupné k vytvoření vazby.
Charakteristika a rozdělení
Nukleofilitu je vhodné odlišit od zásaditosti. Zatímco zásada měří tendenci přijímat proton (H+), nukleofilita popisuje schopnost napadat atomy s elektronovým deficitem. Rozhodující faktory jsou elektrický náboj, polarizovatelnost, dostupnost elektronového páru a sterické překážky. Malé, nabité aniony (např. OH−, Cl−) bývají často silné nukleofily v nepolarizujících podmínkách, zatímco měkčí, polarizovatelné nukleofily (např. I−, RS−) lépe reagují s měkčími elektrofilními centry.
Mechanismy a vliv prostředí
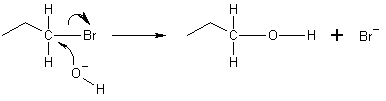
Nukleofily se účastní celé řady reakcí; nejčastější jsou nukleofilní substituce a adice. V organické chemii rozlišujeme například mechanizmy SN1 a SN2 u substitucí. V SN2 probíhá přímo střetnutí nukleofilu s elektrofilním uhlíkem a současné odcházení substituentu, zatímco SN1 zahrnuje vznik karbokationtu před útokem nukleofilu. Solvent hraje významnou roli: polární protické rozpouštědlo (jako alkoholy a voda) může oslabit nukleofilitu stabilizací aniontu, zatímco polární aprotické rozpouštědlo ji často zvýší.
Příklady běžných nukleofilů
- Halogenidové aniony (Cl−, Br−, I−) — časté v substitucích.
- Hydroxid a alkoxidy (OH−, RO−) — silné, často používány pro deprotonování i substituce.
- Aminy (RNH2, NH3) — neutrální nukleofily, zapojují se do adicí a tvorby amonných aduktů.
- Thioláty (RS−) a karbaniony — měkčí nukleofily, důležité v syntézách organické chemie.
Obecně mohou být nukleofily molekuly nebo ionty; jejich společným znakem je osamělý pár nebo jiná oblast vysoké elektronové hustoty, kterou nukleofil odevzdává elektrofilu k vytvoření chemické vazby.
Význam, použití a poznámky
Nukleofily hrají klíčovou roli v syntéze, katalýze a biochemických procesech — od jednoduchých substitucí po složité přesmyky a tvorbu vazeb uhlík–uhlík. Reakce, při nichž rozpouštědlo působí jako nukleofil, se označují jako solvolýza nebo obecně jako nukleofilní reakce. Prakticky orientovaný chemik při volbě nukleofilu zohlední také kvalitu odcházející skupiny, kinetiku reakce a vedlejší procesy. V laboratoři i průmyslu se proto často provádějí testy za různých podmínek, aby se stanovilo, který nukleofil je pro daný účel nejvhodnější.
Užitečné rozlišení a doporučení
- Rozlišujte nukleofilitu (reaktivita směrem k elektrofilu) a zásaditost (reaktivita vůči protónům).
- Uvažujte o rozpouštědle: protická média tlumí nabité nukleofily, aprotická je často zvýhodňují.
- Sterické překážky mohou snížit efektivitu i u silných nukleofilů.
- Pro praktické reakce zvažte i stabilitu vzniklého aduktu a dostupnost odcházející skupiny.
Pro další informace o konkrétních mechanismech a případech použití viz přehledy a výukové zdroje o nukleofilních substitučních reakcích a o jejich aplikacích v organické syntéze.