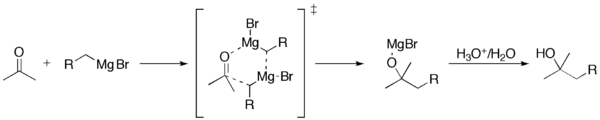
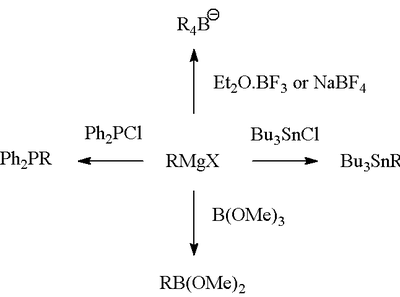
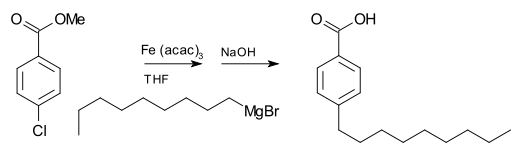
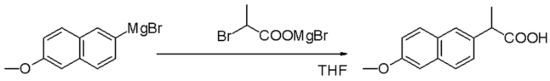
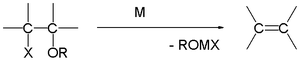
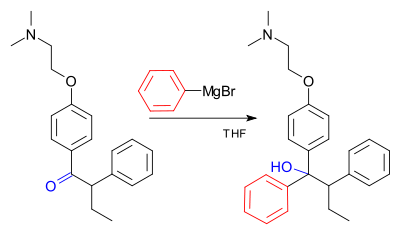
Grignardova reakce (vyslovuje se /ɡriɲar/) je organokovová chemická reakce, při níž alkyl- nebo aryl-halogenidy hořčíku (Grignardova činidla) útočí na elektrofilní atomy uhlíku, které se nacházejí v polárních vazbách (například v karbonylové skupině, jak je uvedeno v příkladu níže). Grignardova činidla působí jako nukleofily. Grignardova reakce vytváří vazbu uhlík-uhlík. Mění hybridizaci kolem reakčního centra. Grignardova reakce je důležitým nástrojem při tvorbě vazeb uhlík-uhlík. Může také vytvářet vazby uhlík-fosfor, uhlík-cín, uhlík-křemík, uhlík-bór a další vazby uhlík-heteroatom.
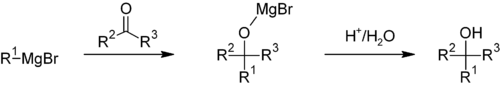
Jedná se o nukleofilní organokovovou adiční reakci. Vysoká hodnota pKa alkylové složky (pKa = ~45) činí reakci nevratnou. Grignardovy reakce nejsou iontové. Grignardovo činidlo existuje jako organokovový klastr (v éteru).
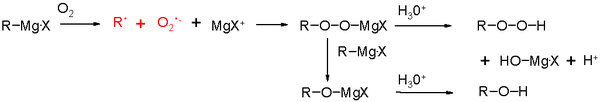
Nevýhodou Grignardových činidel je, že snadno reagují s proaktivními rozpouštědly (např. s vodou) nebo s funkčními skupinami s kyselými protony, jako jsou alkoholy a aminy. Atmosférická vlhkost může změnit výtěžek při výrobě Grignardova činidla z hořečnatého soustruhu a alkylhalogenidu. Jednou z mnoha metod, které se používají k vyloučení vody z reakční atmosféry, je vysušení reakční nádoby plamenem, aby se odpařila veškerá vlhkost, která se poté utěsní, aby se zabránilo návratu vlhkosti. Chemici pak pomocí ultrazvuku aktivují povrch hořčíku tak, aby spotřeboval veškerou přítomnou vodu. To může umožnit tvorbu Grignardových činidel s menší citlivostí na přítomnost vody.
Další nevýhodou Grignardových činidel je, že při reakci s alkylhalogenidy mechanismem SN2 nevytvářejí snadno vazby uhlík-uhlík.
François Auguste Victor Grignard objevil Grignardovy reakce a činidla. Jsou pojmenovány po tomto francouzském chemikovi (univerzita v Nancy, Francie), který za tuto práci získal v roce 1912 Nobelovu cenu za chemii.