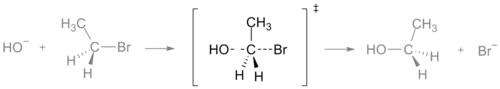V chemické reakci je přechodný stav bod, ve kterém je maximální hodnota energie. Tato energie se nazývá aktivační energie. Když se dvě nebo více molekul smísí, narazí na sebe. Pokud do sebe narazí s dostatečnou energií, aby prošly přechodným stavem, budou reagovat a vytvoří nové molekuly. V přechodném stavu vznikají nové vazby a zároveň se ruší staré. V grafu nebo na obrázku se přechodný stav často označuje symbolem dvojité dýky ‡.
Je velmi obtížné studovat přechodový stav. Je to proto, že má tak vysokou energii, že molekuly v něm setrvají velmi krátkou dobu, obvykle femtosekundy. Je důležité nezaměňovat přechodné stavy s meziprodukty. Meziprodukty se nacházejí v minimálních bodech energie a mohou žít velmi dlouho. Stejně jako přechodný stav se však meziprodukt nachází mezi činidly a produkty reakce.
Studium přechodných stavů je velmi důležité pro pochopení reakčních mechanismů. Existují teorie a počítačové programy, které lze použít k výpočtu toho, jak přechodný stav vypadá. To je součástí chemické kinetiky.