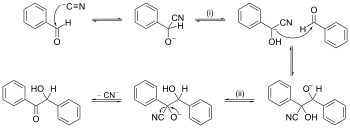
Reakční mechanismus je postupný zápis toho, jak chemická reakce probíhá. Obvykle lze u reakce pozorovat pouze celkovou změnu. Meziprodukty reagují příliš rychle na to, aby byly vidět. Těm se říká meziprodukty a při přechodu z jednoho meziproduktu do druhého se překračuje přechodný stav. Je však důležité pochopit všechny kroky, které tvoří celkovou změnu. Je to proto, že pak lze pochopit složitější reakce nebo se pokusit reakci určitým způsobem přimět k tomu, aby probíhala.
Existuje mnoho typů reakčních mechanismů. V organické chemii jsou nejčastější nukleofilní substituce, eliminace a adice. Lidé někdy používají tlačení šipek, aby nakreslili, jak se elektrony během reakce pohybují. Díky tomu je snadné vidět, které vazby se během procesu vytvářejí a které se přerušují.
Kroky mechanismu a základní pojmy
- Elementární krok – jeden jednoduchý proces, při kterém se mění vazby přímo mezi dvěma nebo více částicemi (např. jedna molekula se rozpadne nebo dvě se srazí a vytvoří novou vazbu). Rychlost elementárního kroku lze přímo vyjádřit jeho kinetickým řádem.
- Meziprodukt – krátkodobě existující sloučenina vznikající mezi kroky. Obvykle má vyšší energii než výchozí látky a je reaktivní.
- Přechodný stav – energie-maximální konfigurace při přechodu mezi meziproduktem a dalším stavem; nelze jej izolovat, pouze popsat energeticky.
- Rychlost určující krok (rate-determining step) – nejpomalejší elementární krok v mechanismu, který určuje celkovou rychlost reakce a tvar kinetické závislosti.
- Koncertované vs. postupné (stepwise) – některé reakce probíhají v jediném, současném (koncertovaném) kroku (např. pericyklické reakce), jiné přes izolovatelné nebo krátkodobé meziprodukty.
Energetický profil a kinetika
Mechanismus se popisuje i pomocí energetického diagramu (energie proti reakčnímu koordinátu). Každý elementární krok má svoji aktivační energii (E_a). Vícekrokové reakce mají několik vrcholů (přechodných stavů) a někdy i lokální minima reprezentující meziprodukty. Termodynamika (rozdíl energie mezi výchozími látkami a produkty) určuje, zda je reakce celkově výhodná, zatímco kinetika (velikost aktivačních energií) určuje, jak rychle proběhne.
Příklady běžných mechanismů v organické chemii
- Nukleofilní substituce – dvě hlavní varianty: SN2 (koncertovaný jednorázový útok nukleofilu při současném odcházení skupiny; typicky u primárních a methyl derivátů) a SN1 (dvou-krokový: nejprve odchází skupina a vzniká karbokation, poté se váže nukleofil; typické pro terciární centrum). Příklad SN2: CH3Br + OH− → CH3OH + Br−.
- Eliminace – E2 (koncertovaný odchod protonu a lepší odcházející skupiny; závisí na stereochemii) a E1 (dvoustupňová, přes karbokation). Výsledkem je vznik dvojné vazby.
- Adice – k násobným vazbám (např. elektrofilní adice na alkeny), často probíhá přes elektrofilní útok následovaný nukleofilním zásahem.
- Radikálové mechanismy – iniciace, propagace, terminace; typické pro halogenace alkanů nebo polymerizace.
Co ovlivňuje průběh mechanismu
- síla a koncentrace nukleofilu nebo elektrofilu,
- kvalita a stabilita odcházející skupiny,
- sterické a elektronové efekty v substrátu (např. substituce, rezonance),
- rozpouštědlo (polární protické vs. aprotické může upřednostnit SN1 nebo SN2),
- teplota (zvyšuje rychlost a může změnit poměr konkurujících cest),
- přítomnost katalyzátorů (např. kyseliny, zásady, kovové katalyzátory) – často mění mechanismus snížením aktivační energie.
Jak se mechanismy zjišťují experimentálně
- Kinetické studie – měřením závislosti rychlosti na koncentracích lze odhadnout elementární kroky a jejich pořadí.
- Izotopové značení (např. D, 13C) – sleduje přesun atomů a pomáhá odlišit různé cesty (kinetický izotopový efekt).
- Trapping meziproduktů – použitím reaktantů, které zachytí krátkodobé meziprodukty, umožní jejich identifikaci.
- Spektroskopie a chromatografie – NMR, IR, MS, UV–Vis a GC/MS pro sledování mezistavů a produktů v reálném čase.
- Výpočtová chemie – kvantově-chemické výpočty pro mapování energetických povrchů a odhad přechodných stavů.
Praktický význam porozumění mechanismům
Pochopení mechanizmu umožňuje chemikům:
- navrhovat podmínky, které zvýší výtěžek nebo selektivitu,
- vyhnout se vedlejším reakcím,
- vyvíjet nové katalyzátory nebo reaktanty,
- interpretuje experimentální data a předpovívat produkty v nových situacích.
Souhrnně: reakční mechanismus není jen popis „co“ vznikne, ale podrobný návod „jak“ a „proč“ reakce probíhá. Díky tomu lze chemické procesy lépe ovládat a využívat v syntéze, průmyslu i výzkumu.