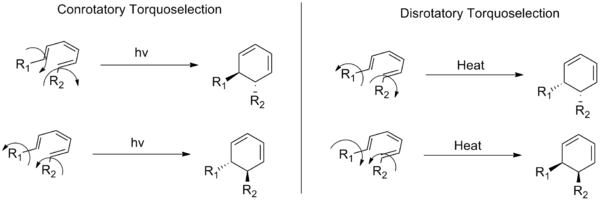
Tyto termíny popisují dvě třídy elektrocyklických reakcí (typ organických chemických reakcí). V konrotativním režimu se substituenty umístěné na koncích konjugovaného systému dvojných vazeb pohybují při otevírání nebo uzavírání kruhu ve stejném směru (ve směru nebo proti směru hodinových ručiček). V disrotačním režimu se pohybují v opačném směru.
Příkladem je přeměna trans-cis-trans-2,4,6-oktatrienu na cis-dimethylcyklohexadien (nahoře na obrázku). Orbitální mechanika reakce vyžaduje disrotační režim. Orbitální symetrie nejvýše obsazeného molekulového orbitalu oktatrienu (HOMO) vyžaduje, aby se koncové orbitaly pí pohybovaly v opačných směrech, aby se vytvořila správná symetrie, která se nachází ve vazbě sigma.
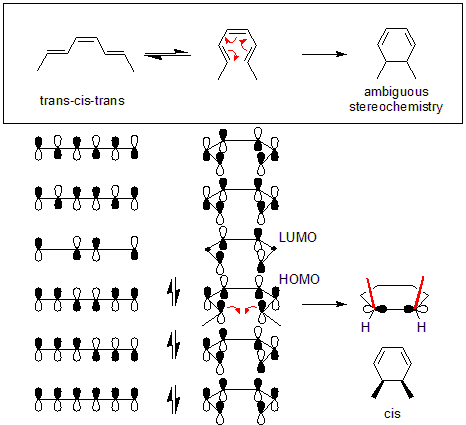
Tepelné přestavby všech konjugovaných systémů obsahujících 4n + 2 pi elektronů jsou stereospecifické. To je založeno na zachování orbitální symetrie v nejvyšším obsazeném molekulovém orbitalu. Systémy obsahující 4n elektronů pí vykazují opačný konrotativní režim. To platí i pro přeskupení 4n + 2 pi (kde n je celé číslo) elektronů řízené světlem (fotoindukované). Fotoindukované přeskupení systémů se 4n pi elektrony (kde je počet elektronů dělitelný 4) se řídí disrotačním pravidlem.
Woodwardova-Hoffmannova pravidla shrnují výše uvedené různé reakce.
Následující obrázek také ukazuje rozdíl mezi konrotativními a disrotativními reakcemi: