Otázka: Co je to aromatický uhlovodík?
Odpověď: Aromatický uhlovodík je uhlovodíková kruhová sloučenina se střídajícími se dvojnými a jednoduchými vazbami mezi atomy uhlíku tvořícími kruhy a mnohé z těchto sloučenin mají sladkou vůni.
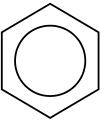
Otázka: Jak se nazývá kruh o šesti atomech uhlíku v aromatických sloučeninách?
Odpověď: Kruh šesti atomů uhlíku v aromatických sloučeninách se nazývá benzenový kruh.
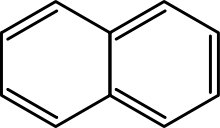
Otázka: Jaký je rozdíl mezi monocyklickými (MAH) a polycyklickými (PAH) aromatickými uhlovodíky?
Odpověď: Monocyklické aromatické uhlovodíky (MAH) mají ve své struktuře jeden kruh atomů uhlíku, zatímco polycyklické aromatické uhlovodíky (PAH) mají ve své struktuře dva nebo více spojených kruhů atomů uhlíku.
Otázka: Proč se aromatické uhlovodíky nazývají "aromatické"?
Odpověď: Aromatické uhlovodíky se nazývají "aromatické", protože mnohé z nich mají sladkou vůni.
Otázka: Co jsou to heteroareny a jak se liší od aromatických sloučenin na bázi benzenu?
Odpověď: Heteroareny jsou sloučeniny, které nejsou na bázi benzenu a řídí se Hückelovým pravidlem, a které jsou také aromatickými sloučeninami. V těchto sloučeninách je alespoň jeden atom uhlíku nahrazen jedním z atomů kyslíku, dusíku nebo síry.
Otázka: Jaký je nejjednodušší možný uhlovodíkový kruh?
Odpověď: Nejjednodušší možný uhlovodíkový kruh je benzen.
Otázka: Jaké jsou dva typy aromatických uhlovodíků?
Odpověď: Dva typy aromatických uhlovodíků jsou monocyklické (MAH) a polycyklické (PAH) aromatické uhlovodíky.