Aminokyseliny jsou stavebními kameny bílkovin. U eukaryot existuje 20 standardních aminokyselin, z nichž se skládají téměř všechny bílkoviny.
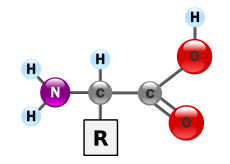
V biochemii je aminokyselina jakákoli molekula, která má aminovou (NH2+R) a karboxylovou (C=O) funkční skupinu. V biochemii se tento termín vztahuje na alfa-aminokyseliny s obecným vzorcem H2NCHRCOOH, kde R je jedna z mnoha postranních skupin (viz schéma).
Je známo přibližně 500 aminokyselin. Pro živočichy je nejdůležitější, že z aminokyselin vznikají bílkoviny, což jsou velmi dlouhé řetězce aminokyselin. Každá bílkovina má svou vlastní sekvenci aminokyselin a tato sekvence způsobuje, že bílkovina má různé tvary a různé funkce. Aminokyseliny jsou pro bílkoviny jako abeceda; i když máte jen několik písmen, když je spojíte, můžete vytvořit mnoho různých vět.
Devět z 20 standardních aminokyselin je pro člověka "esenciálních". Lidské tělo si je nedokáže vytvořit (syntetizovat) z jiných sloučenin, a proto je musí přijímat potravou. Další mohou být nezbytné pro určitý věk nebo zdravotní stav. Esenciální aminokyseliny se mohou lišit i mezi jednotlivými druhy. Býložravci musí esenciální aminokyseliny získávat ze své stravy, kterou u některých druhů tvoří téměř výhradně tráva. Přežvýkavci, jako jsou krávy, získávají některé aminokyseliny prostřednictvím mikrobů v prvních dvou komorách žaludku.
Struktura a základní vlastnosti
Aminokyseliny mají obecnou strukturu: centrální alfa-uhlík (Cα) vázaný na aminovou skupinu (-NH2), karboxylovou skupinu (-COOH), vodík a postranní řetězec označovaný jako R. U většiny aminokyselin je Cα asymetrický (kromě glycinu), což dává vznik dvěma enantiomerům (L- a D-forma). Proteiny u organismů jsou tvořeny prakticky výhradně z L-izomerů.
V neutrálním vodném prostředí se aminokyseliny vyskytují jako zvířené ionty (zwitteriony): aminová skupina je částečně protonovaná a karboxylová deprotonovaná. Hodnoty pKa skupin ovlivňují nabití R-skupiny a tím i rozpustnost a interakce aminokyseliny.
Klasifikace aminokyselin
- Podle polarity R-skupiny: nepolární (hydrofobní), polární neutrální, polární nabité (základní nebo kyselé).
- Speciální typy: aromatické (fenylalanin, tryptofan, tyrosin), obsahující síru (cystein, methionin), imino (prolin), achirální (glycin).
- Podle biologické role: standardní proteinogenní (20 v genetickém kódu), neproteinogenní (mj. modifikované nebo vzácné v proteinech), volné metabolity (např. neurotransmitery).
Role v bílkovinách a v organismu
Aminokyseliny se spojují peptidovou vazbou mezi karboxylovou skupinou jedné a aminovou skupinou druhé aminokyseliny, přičemž vzniká řetězec – polypeptid. Sekvence aminokyselin (primární struktura) určuje sekundární (alfa-helix, beta-skládaný list), terciální (tvar jedné podjednotky) a kvartérní strukturu (složené komplexy více podjednotek).
Funkce aminokyselin a bílkovin v organismu jsou velmi rozmanité:
- strukturální (kolagen, keratin),
- enzymatické (působí jako katalyzátory biochemických reakcí),
- transportní (hemoglobin, transportní proteiny v membránách),
- signální (hormony – např. inzulin je peptidový hormon),
- neurotransmitery a jejich prekurzory (např. tryptofan → serotonin, tyrosin → dopamin, norepinefrin),
- metabolické (zdroj dusíku, zapojení do ureového cyklu, glukoneogeneze při hladovění).
Esenciální a podmíněně esenciální aminokyseliny
Pro dospělého člověka se za esenciálních považuje devět aminokyselin, které musí být získány z potravy:
- Histidin
- Isoleucin (isoleucín)
- Leucin (leucín)
- Lysin (lyzín)
- Methionin (methionín)
- Fenylalanin
- Threonin (threonín)
- Tryptofan (tryptofán)
- Valin
Některé aminokyseliny jsou podmíněně esenciální – tělo je obvykle syntetizuje, ale za určitých stavů (růst, onemocnění, předčasnost novorozenců) je jejich příjem v potravě nutný. Patří sem např. arginin, cystein (odvozen z methioninu), tyrosin (odvozen z fenylalaninu) a další.
Potravní zdroje a doporučení
Dobré zdroje všech esenciálních aminokyselin jsou živočišné bílkoviny: maso, ryby, vejce, mléčné výrobky. Mezi rostlinnými zdroji jsou kompletní bílkoviny sója a quinoa; jinak rostlinné zdroje doplňují své aminokyselinné spektrum kombinací (např. obiloviny + luštěniny).
Doporučený denní příjem bílkovin pro průměrného dospělého je přibližně 0,8 g/kg tělesné hmotnosti; potřeba se zvyšuje u sportovců, těhotných žen a při některých onemocněních. Kvalita bílkovin se hodnotí podle obsahu a poměru esenciálních aminokyselin.
Mimo standardní aminokyseliny a posttranslační modifikace
Kromě 20 standardních existují v proteinech vzácné aminokyseliny, které vznikají během translace (např. selenocystein, pyrrolysine) nebo posttranslačními úpravami (hydroxyprolin v kolagenu). Běžné modifikace R-skupin zahrnují fosforylaci, metylaci, acetylaci, glykozylaci a mnoho dalších, které regulují aktivitu a lokalizaci proteinů.
Krátké shrnutí
Aminokyseliny jsou klíčové pro stavbu a funkci živých organismů. Jejich rozmanitost a pořadí v polypeptidových řetězcích umožňují vzniku širokého spektra proteinových struktur a funkcí. Z hlediska výživy je důležité zajistit přísun esenciálních aminokyselin potravou, zvláště při speciálních nutričních potřebách.