Teplo může způsobit, že dvojné vazby vytvoří kruh. Tepelné cykloadice mají obvykle (4n + 2) π elektronů, které se účastní výchozího materiálu, pro určité celé číslo n. Vzhledem k orbitální symetrii je většina cykloadiccí suprafaciálních. Zřídka jsou antarafaciální-antarafaciální. Existuje několik příkladů tepelných cykloadicí, které mají 4n π elektronů (například cykloadice [2 + 2]). Ty probíhají ve smyslu suprafaciální-antarafaciální. Například dimerizace ketenu má ortogonální sadu p orbitalů. Tyto p orbitaly umožňují, aby reakce probíhala pomocí zkříženého přechodového stavu.
Světlo může také způsobit, že dvojné vazby vytvoří kruh. V důsledku fotochemické aktivace může dojít také k cykloadici, které se účastní 4n π elektronů. Zde jedna složka způsobí přesun elektronu z nejvýše obsazeného molekulového orbitalu (HOMO) (π vazba) na nejnižší neobsazený molekulový orbital (LUMO) (π* antivazba). Poté, co elektron postoupí do vyššího orbitalu, umožňuje orbitální symetrie, aby reakce probíhala nadfázově-nadfázově. Příkladem je DeMayova reakce. Další příklad je uveden níže, fotochemická dimerizace kyseliny skořicové.
Všimněte si, že ne všechny fotochemické (2+2) cyklizace jsou cykloadicemi; o některých je známo, že probíhají radikálovým mechanismem.
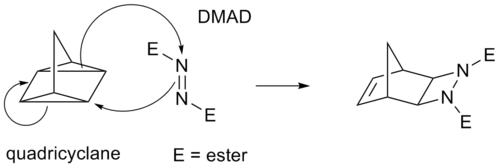
Některé cykloadice namísto π vazeb probíhají přes napjaté cyklopropanové kruhy, které mají výrazný π charakter. Analogem Dielsovy-Alderovy reakce je například reakce kvadricyklan-DMAD:
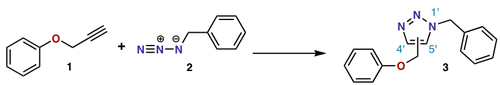
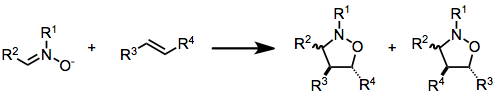
V zápisu (i+j+...) cykloadice i a j označují počet atomů, které se cykloadice účastní. V tomto zápisu je Dielsova-Alderova reakce (4+2)cykloadicí a 1,3-dipolární adice, jako je první krok při ozonolýze, je (3+2)cykloadicí. Tento zápis používá závorky. IUPAC však upřednostňuje zápis [i+j+...], který počítá elektrony, nikoliv atomy. Používá hranaté závorky. V tomto zápisu se Dielsova-Alderova reakce i dipolární reakce stávají [4+2]cykloadicí. Reakce mezi norbornadienem a aktivovaným alkynem je [2+2+2]cykloadice.
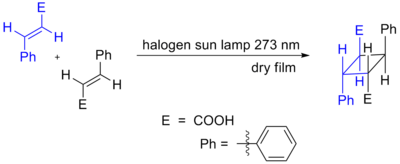
.png)
![Intermolecular Formal [3+3] Cycloaddition Reaction](https://www.alegsaonline.com/image/600px-3+3-cycloaddition.svg.png)