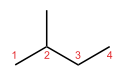Strukturní izomerie (IUPAC ji nazývá konstituční izomerie) je druh izomerie. Dvě chemické látky v této izomerii mají stejný molekulový vzorec, ale molekuly jsou vzájemně spojeny v odlišném pořadí — tedy vazby mezi atomy se liší. Opakem strukturní izomerie je stereoizomerie, kde se liší prostorové uspořádání stejných vazeb. Strukturní izomery často vykazují rozdílné fyzikální a chemické vlastnosti (bod varu, rozpustnost, reaktivitu), proto jsou důležité v organické chemii i v průmyslu.
Druhy konstitučních izomerů
- Skeletové (řetězové) izomery — liší se uspořádáním uhlíkového řetězce (lineární vs větvený řetězec). Příklad: n-butan a isobutan (C4H10).
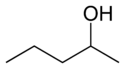
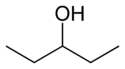
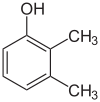
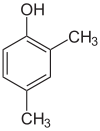
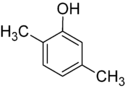
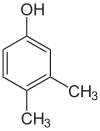
- Polohové (regioizomery) — obsahují stejnou funkční skupinu, ale v různé poloze na kostře molekuly. Příklady: 1-butanol vs 2-butanol, nebo ortho-/meta-/para-dichlorbenzen (různé polohy substituentů na benzenovém jádru).
- Funkční (funkční skupinové) izomery — mají rozdílné funkční skupiny přestože mají stejný celkový složení atomů. Klasický příklad: ethanol (alkohol) a dimethyléter (éter) — oba C2H6O, ale jiné funkční skupiny a jiné vlastnosti. Do této kategorie patří i tautomery, tj. izomery v rychlé rovnováze (např. keto–enol tautomérie u některých karbonylových sloučenin; u β‑diketónů může být enolová forma významná).
Příklady a četnost izomerů
- Skeletové izomery: pro C4H10 existují 2 izomery (n‑butan, isobutan). S růstem počtu uhlíků roste i počet konstitučních izomerů exponenciálně (počet známých izomerů alkanů: C4 → 2, C5 → 3, C6 → 5, C7 → 9, C8 → 18, C9 → 35, C10 → 75 atd.).
- Polohové izomery: u halogenovaných uhlovodíků nebo alkoholů stačí posun skupiny po řetězci — vlastnosti se mění např. bodem varu a reaktivitou.
- Funkční izomery: kromě ethanol / dimethyléter lze uvést propanal (aldehyd) a propanon (keton) jako funkční izomery se vzorcem C3H6O.
Jak izomery odlišit
- Fyzikální vlastnosti — rozdílné body varu, tání, hustota nebo zápach mohou napovědět, o který izomer jde.
- Spektroskopie — IR (odhalí specifické funkční skupiny), NMR (ukáže prostředí atomů vodíku a uhlíku) a MS (různé fragmentační vzory) jsou nejčastějšími metodami rozlišení.
- Chemické reakce — reakční selektivita a produkty se mohou lišit podle typu izomeru (např. reaktivita primárního vs sekundárního alkoholu).
Význam v praxi
Konstituční izomerie ovlivňuje vlastnosti léčiv, rozpouštědel, polymerů a paliv. Různé izomery téže sumární formule mohou mít zcela odlišnou biologickou aktivitu či toxicitu, proto je přesné stanovení struktury zásadní v syntéze a analýze látek.
Krátké shrnutí: Konstituční (strukturní) izomerie = stejný molekulový vzorec, odlišné uspořádání vazeb. Hlavní typy: skeletové, polohové (regioizomery) a funkční (včetně tautomerů). Rozlišení se provádí fyzikálně-chemickými metodami a má praktický význam v chemii i farmacii.