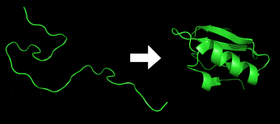
Skládání bílkovin je proces, při kterém bílkovina nabývá svého funkčního tvaru neboli konformace. Je to v zásadě samoorganizační jev: lineární řetězec polypeptidů opouští náhodný závit a přechází do pořádané struktury, kterou často stabilizují například vodíkové vazby a další fyzikálně‑chemické interakce.
Co určuje výslednou strukturu
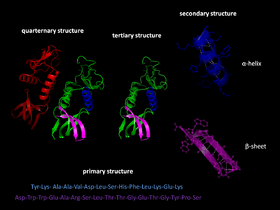
Primární informaci o tom, jak se protein složí, nese pořadí aminokyselin v jeho sekvenci. Ve zjednodušené podobě toto pravidlo vyjadřuje Anfinsenovo dogma, které říká, že sekvence aminokyselin určuje nativní trojrozměrnou strukturu za daných podmínek.
Silové působení a stabilizace
- hydrofobní interakce — často hlavní hnací síla skládání;
- vodíkové vazby — přispívají k sekundární a terciární stabilitě (uvedeno výše jako vodíkové vazby);
- iontové interakce (solné můstky) a elektrostatika;
- disulfidické můstky mezi cysteinovými zbytky;
- van der Waalsovy síly a prostorové zaplnění.
Fáze skládání
- Nově syntetizovaný řetězec: Každý protein se po translaci obvykle objeví jako nenavázaný polypeptid nebo jako relativně náhodná spirála. Tento řetězec je tvořen jednotkami — aminokyselinami — a ještě nemá plně vyvinutou trojrozměrnou strukturu.
- Tvorba nativní struktury: Postupem času vzájemná působení mezi aminokyselinami vedou k ustavení přesné trojrozměrné struktury, která se označuje jako nativní stav. Tento princip předpokládá, že informace o nativním stavu je obsažena v sekvenci (Anfinsenovo dogma).
Pomocné systémy a kinetika
Proces skládání není vždy jednoduchou cestou k energetickému minimu: existuje více mezistavů a možnost tvorby agregátů. Buňky proto využívají molekulární chaperony, které zabraňují neřízené agregaci a pomáhají dosáhnout správné konformace. Skládání se popisuje také pomocí konceptu energetického landscapu, kde cesta k nativnímu stavu může být rozvětvená a kineticky regulovaná.
Části bez pevné struktury
Některé části proteinů mohou zůstat flexibilní nebo nestrukturované i v nativním stavu. Takové intrinsicně nestrukturované oblasti (IDR) jsou běžné a často mají funkci v regulaci, interakcích nebo vázání partnerů; jejich neschopnost vytvořit pevnou trojrozměrnou strukturu tedy není nutně chybou.
Nesprávné skládání a jeho následky
Proteiny, které se nesloží do správné konformace, bývají neaktivní a mohou být toxické. Předpokládá se, že některé nemoci jsou důsledkem hromadění nesprávně složených proteinů. Dále mnoho alergií je způsobeno tím, že imunitní systém reaguje na specifické konformace nebo fragmenty proteinů — proto role konformace v rozpoznání antigenu není zanedbatelná. Imunitní odpověď proti nekorektním nebo cizím strukturám řídí také imunitní systém, který nerozpoznává všechny možné konformace jako neškodné.
Studium a aplikace
- Experimentální metody: rentgenová krystalografie, NMR spektroskopie a kryo‑elektronová mikroskopie (cryo‑EM) patří mezi hlavní nástroje pro určování struktur.
- Výpočetní metody: modelování a predikce konformací se rychle zlepšují a nacházejí uplatnění v biotechnologii a vývoji léčiv.
- Praktický význam: porozumění skládání je klíčové pro pochopení funkcí proteinů, vývoj terapií proti chorobám spojeným s agregací a pro návrh stabilních terapeutických proteinů.