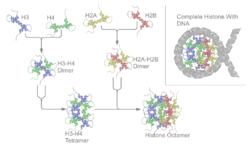
Histony jsou bílkoviny, které se nacházejí v jádrech eukaryotických buněk a které balí DNA do strukturních jednotek zvaných nukleozomy. Jsou hlavními bílkovinnými složkami chromatinu, aktivní složky chromozomů.
Histony fungují jako cívky, kolem nichž se DNA obtáčí, a hrají roli v regulaci genů. Bez histonů by byla odvíjená DNA v chromozomech velmi dlouhá. Například každá lidská buňka má asi 1,8 metru DNA, ale navinutá na histonech má asi 90 milimetrů chromatinu, který při duplikaci a kondenzaci během mitózy vytváří asi 120 mikrometrů chromozomů.
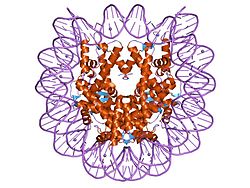
Struktura nukleozomu
Základní strukturní jednotkou chromatinu je nukleozom. Nukleozom tvoří histonový oktamer složený ze dvou kopií každého z histonů H2A, H2B, H3 a H4, kolem kterého se obtáčí přibližně 147 párů bází DNA (asi 1,65 otáčky). Mezi nukleozomy se nachází krátký úsek volné (linker) DNA, ke kterému se váže tzv. linkerový histon H1, který stabilizuje uspořádání a ovlivňuje vyšší stupeň kondenzace chromatinu. Délka linkeru (nukleozomový repeat) je proměnlivá a u různých organismů i typů buněk bývá v rozmezí přibližně 160–240 bp.
Typy histonů a varianty
- Jaklasické histony: H2A, H2B, H3 a H4 tvoří jádro nukleozomu; H1 je linkerový histon.
- Varianty histonů: existují speciální izoformy, např. H3.3 (spojená s aktivním transkriptem), H2A.Z (ovlivňuje stabilitu nukleozomu a transkripci), macroH2A (vzhledem k většímu C-koncovému úseku uplatněná v inaktivaci X), a CENP‑A (specifická pro centromery). Varianty často mění vlastnosti chromatinu a cílují specifické biologické procesy.
Post-translační modifikace a „histonový kód“
Histony mají na svých N- a C-koncích tzv. ocas, které podléhají četným post-translačním modifikacím (PTM). Mezi nejčastější patří:
- acetylace lysinů (HATs jako „writer“; HDACs jako „eraser“) – často koreluje s otevřeným chromatinem a aktivní transkripcí;
- metylace lysinů a argininů – může znamenat aktivaci i repressi v závislosti na místě (např. H3K4me3 je spojeno s aktivací, H3K27me3 s represí);
- fosforylace – například během mitózy nebo při reakci na poškození DNA;
- ubiquitinyace, SUMOylace a další méně časté modifikace.
Soubor těchto modifikací nazýváme někdy histonovým kódem: speciální „čtečky“ (bromodomény, chromodomény aj.) rozpoznávají jednotlivé modifikace a přivolávají proteiny, které mění strukturu chromatinu a regulují transkripci, replikaci a opravu DNA.
Úroveň organizace chromatinu
Komprese DNA probíhá ve vícestupňovém uspořádání:
- nukleozom (základní jednotka),
- uspořádání nukleozomových vláken – existuje model 10 nm „perly na niti“; model 30 nm vlákna je dříve navržený, ale jeho existence in vivo je dnes předmětem diskuse,
- smotky a smyčky chromatinových vláken tvořené pomocí proteinů jako cohesin a CTCF,
- topologicky asociované domény (TADs) a větší chromatické kompartmenty (aktivní A vs. inaktivní B).
Funkce histonů v genomu
- Kondenzace a ochrana DNA: histony zmenšují objem genomu a fyzicky chrání DNA před poškozením.
- Regulace genové exprese: modifikace histonů a přítomnost variant rozhodují, jestli bude oblast chromatinu přístupná pro transkripční faktory a RNA polymerázu.
- Replikace a dělení buněk: histony jsou nově syntetizovány během S-fáze; histonové chaperony pomáhají sestavovat nukleozomy za replikujících vidlic.
- Oprava DNA a stabilita genomu: modifikace histonů přitahují opravných faktorů a mění strukturu chromatinu nutnou pro opravu zlomů.
- Epigenetické dědictví: některé histonové úpravy a varianty se mohou přenášet do dceřiných buněk a ovlivňovat genovou expresi bez změny sekvence DNA.
Dynamika chromatinu: chaperony a remodelační komplexy
Uspořádání nukleozomů není statické. Existují histonoví chaperoni (ASF1, CAF-1 apod.), kteří pomáhají skládat nebo odstraňovat histony, a ATP-dependentní remodelační komplexy (SWI/SNF, ISWI, CHD, INO80), které posunují nebo odstraňují nukleozomy, aby umožnily nebo zamezily přístup transkripčních strojů.
Histony v nemoci a klinickém kontextu
Změny v histonech a enzymatických systémech, které je modifikují, jsou spojeny s různými chorobami:
- mutace v histonových genech (např. H3K27M) jsou spojeny s některými nádory mozku,
- poruchy v histon-modifikujících enzymách (methyltransferázy, deacetylázy) se podílejí na vzniku a progresi rakoviny a jiných onemocnění,
- léčiva cílící HDACs nebo jiné epigenetické enzymy se používají jako terapie u některých typů nádorů a neurologických onemocnění.
Metody studia histonů a chromatinu
- ChIP‑seq: mapuje polohu konkrétních histonových modifikací nebo histonů v genomu.
- MNase‑seq: určuje pozice nukleozomů enzymatickou štěpnou analýzou.
- ATAC‑seq: zjišťuje oblasti otevřeného chromatinu.
- Hmotnostní spektrometrie: identifikuje a kvantifikuje post‑translační modifikace histonů.
- Strukturní metody: rentgenová krystalografie a kryo-EM odhalují vysokou rozlišovací strukturu nukleozomu a komplexů s dalšími proteiny.
Význam a závěr
Histony nejsou jen „obal“ DNA — jsou aktivní součástí regulace genomu. Kombinace jejich strukturálních vlastností, variant a chemických modifikací umožňuje buňkám dynamicky zapisovat a číst epigenetické informace, koordinovat replikaci a opravy a řídit genetické programy během vývoje a reakce na prostředí. Studium histonů a chromatinu je proto klíčové pro pochopení molekulárních mechanismů zdraví i nemoci.