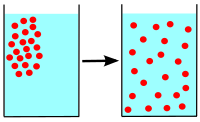
Difuze je fyzikálně-chemický proces, při kterém se molekuly nebo částice látky náhodným tepelným pohybem (Brownovým pohybem) přemisťují z oblasti s vyšší koncentrací do oblasti s nižší koncentrací, až do dosažení rovnovážného rozložení (stejné střední koncentrace všude). Difuze probíhá v plynech, kapalinách i v pevných látkách (i když v pevné fázi je zpravidla mnohem pomalejší). Je to typicky pasivní proces — nevyžaduje přímý přívod energie — a směřuje „po“ koncentračním gradientu (od vyšší koncentrace k nižší).
Obsah
1 Příklady
2 Rychlost difuze a faktory
3 Plocha povrchu a objem
4 Matematický popis
5 Související procesy a aplikace
6 Odkazy
Příklady
- Kostka cukru se nechá v kádince s vodou a její částice (ionty/částečky cukru) se postupně rozptýlí po celém objemu.
- Zápach čpavku se šíří z přední části třídy až do zadních lavic.
- Po sejmutí víčka z lahvičky stoupají výpary parfému a vůně se difuzí rozšíří do místnosti.
- Potravinářské barvivo nakapané do kádinky s vodou se postupně rozptýlí a zabarví celý roztok.
- Vůně jídla se šíří celým domem díky difuzi a proudění vzduchu.
- V biologii: v plicích je více kyslíku než v krvi, takže částice kyslíku difundují do krve; naopak oxid uhličitý difunduje z krve do plic.
- V materiálovém inženýrství a metalurgii probíhá difuze atomů v pevné mřížce (např. při žíhání, tvrdění povrchů nebo dopování polovodičů).
Molekuly se pohybují náhodně; když jsou častěji ve vyšší koncentraci na jednom místě, vyšší pravděpodobnost náhodného pohybu způsobí, že se střední proudění částic bude vyrovnávat směrem do míst s nižší koncentrací. V buňkách malé molekuly často procházejí přes buněčnou membránu jednoduchou difuzí, zatímco větší a nabité molekuly obvykle potřebují speciální kanály nebo energii (viz aktivní transport).
Rychlost difuze a faktory, které ji ovlivňují
Rychlost (nebo intenzita) difuze závisí na řadě faktorů:
- Koncentrační gradient – čím větší rozdíl koncentrací mezi dvěma oblastmi, tím rychlejší je difuze (silnější „tlačná“ síla směrem k vyrovnání).
- Teplota – při vyšších teplotách mají částice větší kinetickou energii, častěji narážejí a rychleji se pohybují, což zvyšuje difuzní rychlost.
- Velikost a hmotnost částic – menší a lehčí částice difundují rychleji než velké a těžké (molekulová hmotnost snižuje difuzní koeficient).
- Viskozita a vlastnosti prostředí – v hustších nebo viskóznějších médiích (např. husté směsi nebo polymery) je difuze pomalejší než ve vzduchu nebo vodě.
- Plocha rozhraní – větší kontaktní plocha mezi oblastmi usnadní větší celkový tok částic.
- Difuzní vzdálenost – doba potřebná k difuzi roste s kvadrátem vzdálenosti; proto difuze na krátké vzdálenosti probíhá relativně rychleji než na dlouhé.
- pH, iontová síla a chemické interakce – v roztocích mohou elektrostatické síly, vazby a komplexace ovlivnit volnost pohybu látek.
- Turbulentní proudění – v tekutinách proudění (konvekce, míchání) může mnohonásobně zrychlit mísení oproti čisté molekulární difuzi.
Plocha povrchu a poměr povrchu k objemu
U malých jednobuněčných organismů stačí často jednoduchá difuze k výměně plynů a živin, protože mají vysoký poměr povrchu k objemu — relativně velká vnější plocha umožňuje rychlou výměnu na jednotku objemu. U větších mnohobuněčných organismů sama difuze nestačí k distribuci látek na větší vzdálenosti, a proto se vyvinuly specializované transportní systémy (např. krevní oběh u živočichů, cévní systém u rostlin, plicní alveoly pro výměnu plynů), které kombinují difuzi na lokální úrovni s konvekcí a řízeným transportem.
Matematický popis (základy)
Pro kvantitativní popis difuze se používají Fickovy zákony:
- Fickův první zákon (stacionární stav): tok částic J (množství látky přecházející plochou za jednotku času) je úměrný negativnímu gradientu koncentrace:
J = -D (dc/dx),
kde D je difuzní koeficient (difuzivita), dc/dx je prostorový gradient koncentrace. - Fickův druhý zákon (časová změna koncentrace): popisuje, jak se koncentrace mění v čase v závislosti na druhé derivaci podle prostoru a difuzním koeficientu:
∂c/∂t = D ∂²c/∂x² (v nejjednodušším homogenním případě).
Difuzní koeficient D závisí na teplotě, viskozitě prostředí a velikosti částice. Pro mnohé systémy platí přibližné Arrheniovo závislostní vyjádření:
D = D0 · exp(-Ea/(kT)),
kde Ea je aktivační energie difuze, k Boltzmannova konstanta a T absolutní teplota.
Související procesy a aplikace
- Osmóza je speciální případ přesunu rozpouštědla (nejčastěji vody) přes polopropustnou membránu v důsledku rozdílu koncentrací rozpuštěných látek.
- Facilitovaná difuze v biologii — průchod větších nebo nabitých molekul přes membránové kanály nebo přenašeče bez přímé spotřeby energie.
- Aktivní transport — přesun látek proti koncentračnímu gradientu za spotřeby energie (na rozdíl od pasivní difuze).
- V průmyslu a technologii: separace plynů, katalýza, výroba polovodičů (dopování), ochrana proti korozi, formulace léčiv a uvolňování léků pomocí difuze.
Difuze je tedy základním mechanismem pro míchání a přesun látek v přírodě i technice. V praxi se často uplatňuje společně s konvekcí a chemickými reakcemi; pochopení jejích zákonitostí je klíčové v chemii, biologii, fyzice i inženýrství.