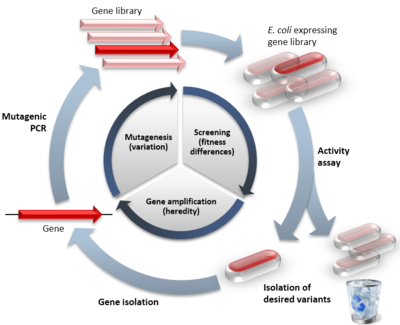
Řízená evoluce (DE) je experimentální metoda používaná k výrobě a optimalizaci enzymů a jiných proteinů pro průmyslové, diagnostické nebo lékařské účely. Jde o praktické proteinové inženýrství, které v laboratorních podmínkách napodobuje principy přirozeného výběru — opakovaně vytváří variace genetické informace, testuje jejich funkci a vybírá ty nejlepší varianty.
Základní principy
Základní myšlenka spočívá v tom, že cílový gen prochází opakovanými koly diverzifikace (mutace, rekombinace) a selekce/screeningu, čímž se vytváří knihovna variant. Pomocí testů se izolují geny s požadovanou funkcí a tyto vítězné varianty slouží jako předlohou pro další kolo evoluce. Tento cyklus se opakuje, dokud není dosaženo požadované kombinace vlastností (např. vyšší aktivity, stability, specificity nebo změněné substrátové preference).
Metody diverzifikace
K vytvoření variability se používá řada technik:
- Random mutagenesis — např. error-prone PCR, použití mutageních polymeráz (Mutazyme), chemická mutageneze nebo mutátorové bakteriální kmeny. Vytváří náhodné bodové mutace v genomu nebo v cílovém genu.
- Rekombinace — DNA shuffling (fragmentace a znovuskládání), StEP a další rekombinační metody kombinují užitečné motivy z různých rodičovských genů.
- Saturace a cílená mutageneze — místní (site-saturation) mutace pro systematické testování všech aminokyselin na klíčových pozicích.
- Oligonukleotidové knihovny — syntetické knihovny s řízenou variabilitou; umožňují vytvářet menší, ale inteligentně navržené knihovny.
- Kontinuální evoluce — systémy jako PACE (phage-assisted continuous evolution) nebo OrthoRep umožňují nepřetržitou evoluci bez nutnosti manuálních cyklů, což zrychluje získávání adaptací.
Výběr a screening
Po vytvoření knihovny je nutné najít a oddělit žádoucí varianty. Rozlišujeme dvě hlavní strategie:
- Selection — přežívání nebo růst je přímo závislý na žádoucí aktivitě (např. enzym, který rozkládá jediné dostupné uhlíkaté zdroje pro buňku). Výhodou je vysoká propustnost (mnoho variant lze rychle hodnotit), nevýhodou může být nepřesné spojení aktivity s přežitím.
- Screening — jednotlivé varianty jsou testovány přímo (např. měřením aktivity pomocí barviv, fluorescence nebo analytických metod). Screening umožňuje kvantitativní hodnocení, ale je obvykle náročnější na práci a instrumentaci.
Formáty provedení: in vivo versus in vitro
Řízená evoluce lze provádět in vivo i in vitro, přičemž každý přístup má své výhody a omezení.
Během evoluce in vivo je každá buňka (často bakterie nebo kvasinka) transformována plazmidem obsahujícím jiný člen knihovny variant. Mezi buňkami se liší pouze gen, který je předmětem zájmu; ostatní geny a buněčné prostředí zůstávají stejné. Buňky exprimují protein buď v cytoplazmě, nebo na povrchu, kde lze testovat jeho funkci nebo ji svázat se signálem (např. fluorescenčním nebo růstovým). Výhodou je, že výběr probíhá v buněčném kontextu, což je důležité, pokud má být vyvinutý protein použit v živých organismech.
Pokud se DE provádí bez buněk, používá se in vitro transkripční–translatační systém k produkci proteinů nebo RNA volně v roztoku nebo v umělých mikrokapičkách. To má několik výhod: umožňuje širší škálu podmínek (teplota, rozpouštědla, pH), lze exprimovat proteiny toxické pro buňky a často se dosahuje mnohem větších knihoven (až 1015 a více), protože DNA knihovny není nutné vložena do buněk. Metody jako emulzní mikrokompartmentalizace, ribosome display nebo mRNA display umožňují udržet spojení mezi fenotypem (aktivita proteinu) a genotypem (kódující RNA/DNA).
Display technologie a vysokokapacitní metody
Pro efektivní propojení genu a jeho produktu jsou často používány display systémy:
- Phage display — protein je na povrchu bakteriofága, vazba nebo funkce může být selektována pomocí afinity k cílovému ligandu.
- Yeast a bacterial surface display — expresní systém na povrchu buněk; umožňuje použití FACS (fluorescenčního třídění) pro rychlý screening.
- Ribosome a mRNA display — in vitro metody, kde je protein fyzicky spojen s jeho mRNA/ribozomem, umožňují extrémně velké knihovny.
- Microdroplet microfluidics — jednotlivé enzymatické reakce probíhají v separátních kapkách; vhodné pro ultravysoce propustný screening (miliony až miliardy testů).
Cíle optimalizace a parametry
Řízená evoluce může cílit na různé vlastnosti proteinu:
- zvýšení katalytické aktivity nebo Km/kcat optimalizace,
- zvýšení termální nebo chemické stability,
- změna substrátové specificity nebo enantioselektivity,
- snížení inhibice či zlepšení odolnosti vůči proteázám,
- zvýšení expresibility a solubility v produkčním systému.
Pokročilé přístupy a kombinace s výpočetními metodami
V posledních letech se často kombinuje řízená evoluce s výpočetním navrhováním: analýza sekvencí, modelování struktury a strojové učení pomáhají navrhnout menší, účinnější knihovny nebo předpovědět užitečné mutace. Také se používá rekonstukce předků (ancestral sequence reconstruction) nebo dirigované mutageneze založená na konzervaci a pozorování mutačních „horkých míst“.
Aplikace
Řízená evoluce má široké uplatnění:
- průmyslové enzymy pro detergenty, potravinářství, papírenský průmysl a výrobu biopaliv,
- biofarmaka a terapeutické enzymy — zlepšení stability, snížení imunogenicity nebo změna specifity,
- vytváření biosenzorů a diagnostických nástrojů,
- metabolické inženýrství — optimalizace enzymů v biosyntetických cestách pro produkci hodnotných molekul,
- bioremediace — enzymy degradující znečišťující látky nebo plastické polymery.
Praktická omezení a bezpečnost
Při navrhování experimentů je nutné zvážit několik omezení: velikost knihovny je omezena kapacitou clonování nebo screeningových metod, vysoký mutační nátlak může vést k destabilizaci proteinů a je potřeba volit vhodné selekční tlaky, aby bylo dosaženo reálného zlepšení požadovaných vlastností. Dále platí důležitá pravidla biologické bezpečnosti a etiky — experimenty by měly probíhat v odpovídajícím biosafety režimu, často s použitím nepatogenních hostitelů nebo biologických zábran, a podle platných předpisů a interních komisí pro biologickou bezpečnost. Vývoj nových aktivit, zejména pak těch, které by mohly mít potenciálně škodlivé důsledky, vyžaduje pečlivé posouzení rizik a kontrolu.
Závěr
Řízená evoluce je silný nástroj pro modifikaci a optimalizaci enzymů a proteinů obecně. Kombinací vhodných metod diverzifikace, display technik, rychlého screeningu a moderních výpočetních postupů lze dosáhnout významných změn vlastností proteinů v relativně krátkém čase. Správně navržený experiment bere v úvahu jak technické možnosti (knihovny, screening), tak i bezpečnostní a etické aspekty použití upravených proteinů v praxi.