Existuje několik alotropů uhlíku. Nejznámější jsou diamant a grafit. Grafit je vodič, polokov (prvek, který je částečně kovem a nekovem, např. černý fosfor a šedý selen). Lze jej použít například jako materiál elektrod obloukových lamp. Grafit je nejstabilnější forma pevného uhlíku, která byla kdy objevena.
Alotropy jsou různé formy téhož chemického prvku. Všechny prvky jsou tvořeny jedinečnými vlastními atomy. Veškeré fyzikální rozdíly jsou způsobeny tím, jak jsou atomy spojeny dohromady. Mnoho prvků vykazuje alotropii, protože existuje řada způsobů, jak mohou být atomy spojeny dohromady. Také existují různé způsoby, jak mohou být molekuly uspořádány do větších struktur.
Diamant je jedním z nejznámějších alotropů uhlíku. Díky své tvrdosti a vysokému rozptylu světla je vhodný pro použití ve šperkařství. Má také průmyslové využití. Diamant je nejtvrdší známý přírodní minerál. Díky tomu je vynikajícím brusivem. Diamant si také dobře udržuje svůj lesk. Diamant i grafit mají extrémně vysoký bod tání, což je pro nekovový prvek neobvyklé.
Co je alotropie uhlíku a proč jsou vlastnosti tak odlišné
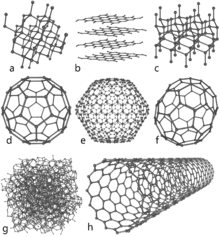
Alotropie znamená, že tentýž chemický prvek může existovat v různých strukturách vázaných jinak mezi sebou. U uhlíku závisí vlastnosti především na typu vazby mezi atomy: sp3 vazby (tetraedrické) vedou k tvrdé trojrozměrné síti diamantu, sp2 vazby (planární) vytvářejí vrstvy v grafitu a grafenu, a sp vazby vedou k lineárním strukturám. Rozdílné prostorové uspořádání elektronů a vazeb dává jednotlivým alotropům zcela odlišné vlastnosti — mechanické, elektrické i optické.
Hlavní alotropy uhlíku a jejich vlastnosti
- Diamant: Krystalická struktura založená na sp3 vazbách. Vlastnosti: extrémní tvrdost (nejtvrdší přírodní minerál), vysoká tepelná vodivost, průhlednost a vysoký index lomu (což dává výrazný lesk u brusu). Elektricky je diamant izolační. Použití: šperkařství, brusné nástroje, řezací a vrtací nástroje, průmyslové a vědecké aplikace (např. tepelný odvod v elektronice u syntetických diamantů).
- Grafit: Skládá se z vrstev grafenu vázaných slabými van der Waalsovými silami; v rámci vrstev jsou atomy v sp2 vazbách. Vlastnosti: měkký, mazavý, vodič elektrického proudu (díky delokalizovaným π-elektronům), odolný proti vysokým teplotám. Použití: elektrody (např. jako materiál elektrod obloukových lamp), tuhy do tužek, maziva, taveninové výstelky, kompozity a grafitové tyče.
- Grafen: Jednovrstvá hexagonální mřížka atomů uhlíku (jeden atom tlustá). Vlastnosti: výjimečná pevnost (vyšší než ocel při nízké hmotnosti), velmi vysoká elektrická a tepelná vodivost, téměř průhledný. Potenciál: elektronika vysoké rychlosti, senzory, kompozity, energetické aplikace.
- Fullereny (např. C60 – Buckminsterfulleren): Uzavřené klece atomů uhlíku připomínající fotbalové míče. Vlastnosti: unikátní chemické vlastnosti, možnost zachycovat atomy/molekuly uvnitř klece, některé deriváty vykazují zajímavé optické a elektronické chování. Použití v materiálovém výzkumu, medicíně (dodávání léčiv), organické elektronice a při studiu supravodivosti.
- Uhlíkové nanotrubice (CNT): Válcové struktury vytvořené svinutým grafenem. Vlastnosti: vysoká tahová pevnost, vynikající elektrická a tepelná vodivost (mohou být kovové nebo polovodičové v závislosti na chiralitě). Použití: kompozity, nanoelektronika, senzory, energetické aplikace.
- Amorfní uhlík: Např. saze, uhlík v uhlí nebo aktivní uhlí – bez dlouhodobého krystalického uspořádání. Vlastnosti závisí na poměru sp2/sp3; typické jsou absorpční vlastnosti, poréznost (aktivní uhlí), nebo tepelná a chemická odolnost. Použití: filtrace, katalýza, absorpční materiály, barviva.
Stabilita a přeměny
Za běžných podmínek (tlak a teplota) je nejstabilnější forma pevného uhlíku grafit. Diamant je termodynamicky metastabilní a při velmi dlouhém čase a vhodných podmínkách by se mohl přeměnit na grafit; v praxi je tato přeměna pomalá, proto diamant vydrží po miliony let. Při vysokém tlaku a teplotě (např. vnitřní zemské procesy nebo průmyslové HPHT podmínky) může grafit přecházet v diamant a naopak.
Výroba a syntéza
Syntetické diamanty se vyrábějí dvěma hlavními způsoby: HPHT (high-pressure high-temperature) — napodobení geologických podmínek, a CVD (chemical vapor deposition) — chemické napařování plynů na substrát, které umožňuje růst tenkých diamantových vrstev a použít je v průmyslu i elektronice. Grafen a uhlíkové nanostruktury se získávají různými metodami (mechanické odtržení, CVD, chemická syntéza či růst z par), přičemž každá metoda ovlivňuje kvalitu a vlastnosti výsledného materiálu.
Přehled praktických použití
- Průmyslové nástroje a brusivo: diamantové břity, kotouče, vrtáky.
- Elektrické a termální aplikace: grafitové elektrody, tepelně vodivé komponenty ze syntetického diamantu.
- Elektronika a nanotechnologie: grafen a uhlíkové nanotrubice pro rychlé tranzistory, senzory, flexibilní elektroniku.
- Lékařství a farmacie: deriváty fullerenu a nanostruktury pro dodávání léčiv a zobrazování.
- Konstrukční materiály: kompozity vyztužené CNT nebo grafenem pro lehké a pevné konstrukce.
- Filtrace a čištění: aktivní uhlí pro adsorpci nečistot a toxinů.
Závěrem
Alotropie uhlíku je jedním z nejpůsobivějších příkladů toho, jak totéž atomové složení může vést k materiálům s dramaticky odlišnými vlastnostmi — od nejtvrdšího přírodního minerálu (diamant) po měkký, mazlavý a elektricky vodivý grafit, přes jednovrstvý grafen s mimořádnými mechanickými a elektronickými vlastnostmi až po složité nanostruktury jako fullereny a uhlíkové nanotrubice. Tyto rozdíly otevírají široké spektrum vědeckých i technologických využití.