Van der Waalsovy síly jsou v chemii typem mezimolekulových sil. Mezimolekulární síla je relativně slabá síla, která drží molekuly pohromadě. Van der Waalsovy síly jsou nejslabším typem mezimolekulových sil. Jsou pojmenovány po nizozemském vědci Johannesi Dideriku van der Waalsovi (1837-1923).
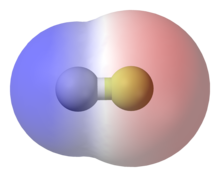
Záporně nabité elektrony obíhají kolem molekul nebo iontů. Elektrony vytvářejí mírně odlišné náboje od jednoho konce molekuly k druhému. Tyto nepatrné rozdíly se nazývají částečné náboje jako δ- nebo δ+.
Tento termín se někdy používá volně jako synonymum pro všechny mezimolekulární síly. Van der Waalsovy síly jsou ve srovnání s kovalentními vazbami relativně slabé, ale hrají zásadní roli v supramolekulární chemii, enzymologii, polymerní vědě, nanotechnologii, povrchové vědě a fyzice kondenzovaných látek. Van der Waalsovy síly určují mnoho vlastností organických sloučenin, včetně jejich rozpustnosti.

