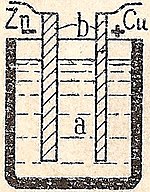
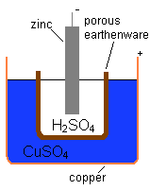
Elektrochemický článek, který způsobuje průtok vnějšího elektrického proudu, lze vytvořit pomocí dvou různých kovů, protože kovy se liší svou tendencí ztrácet elektrony. Zinek ztrácí elektrony snadněji než měď, takže umístění kovového zinku a mědi do roztoků jejich solí může způsobit tok elektronů vnějším vodičem, který vede od zinku k mědi. Když atom zinku poskytne elektrony, stane se kladným iontem a přejde do vodného roztoku, čímž se sníží hmotnost zinkové elektrody. Na straně mědi umožňují dva přijaté elektrony přeměnit měďnatý iont z roztoku na nenabitý atom mědi, který se usazuje na měděné elektrodě, čímž se zvyšuje její hmotnost. Obě reakce se obvykle zapisují
Zn(s) --> Zn2+(aq) + 2e
Cu2+(aq) + 2e ---> Cu(s)
Písmena v závorkách jen připomínají, že zinek přechází z pevné látky (s) do vodného roztoku (aq) a naopak měď. Pro elektrochemii je typické označovat tyto dva procesy jako "poloreakce", které probíhají na obou elektrodách.
| Zn(s) -> Zn2+(aq) + 2e | | "Poloreakce" zinku se klasifikuje jako oxidace, protože ztrácí elektrony. Svorka, na které dochází k oxidaci, se nazývá "anoda". U baterie je to záporný pól. | |
| "Poloreakce" mědi se klasifikuje jako redukce, protože získává elektrony. Svorka, na které dochází k redukci, se nazývá "katoda". U baterie je to kladný pól. | | Cu2+(aq) + 2e- -> Cu(s) |
Aby mohl voltážní článek nadále vyrábět vnější elektrický proud, musí docházet k pohybu síranových iontů v roztoku zprava doleva, aby se vyrovnal tok elektronů ve vnějším obvodu. Samotným kovovým iontům musí být zabráněno v pohybu mezi elektrodami, takže nějaký druh porézní membrány nebo jiný mechanismus musí zajistit selektivní pohyb záporných iontů v elektrolytu zprava doleva.
K tomu, aby se elektrony přesunuly ze zinkové na měděnou elektrodu, je zapotřebí energie a množství energie, které je k dispozici na jednotku náboje voltaického článku, se nazývá elektromotorická síla (emf) článku. Energie na jednotku náboje se vyjadřuje ve voltech (1 volt = 1 joule/coulomb).
Je zřejmé, že k získání energie z buňky je třeba získat více energie uvolněné oxidací zinku, než je třeba k redukci mědi. Článek může z tohoto procesu získat konečné množství energie, přičemž proces je omezen množstvím dostupného materiálu buď v elektrolytu, nebo v kovových elektrodách. Pokud by například na straně mědi byl jeden mol síranových iontů SO42-, pak je proces omezen na přenos dvou molů elektronů vnějším obvodem. Množství elektrického náboje obsaženého v jednom molu elektronů se nazývá Faradayova konstanta a rovná se Avogadrovo číslo krát náboj elektronů:
Faradayova konstanta = F = ANe = 6,022 x 1023 x 1,602 x 10-19 = 96,485 coulombů/mole
Energetický výtěžek voltového článku je dán součinem napětí článku a počtu molů přenesených elektronů krát Faradayova konstanta.
Výstupní elektrická energie = nFE
Emf článku Ecell lze předpovědět ze standardních elektrodových potenciálů pro oba kovy. Pro článek zinek/měď za standardních podmínek je vypočtený potenciál článku 1,1 V.