Přehled
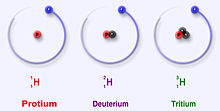
Izotopy vodíku jsou varianty jednoho prvku lišící se počtem neutronů v jádře. Z běžného hlediska rozlišujeme tři hlavní izotopy: nejlehčí a nejrozšířenější protium, těžší deuterium a radioaktivní tritium. Podrobné informace o souhrnu izotopů vodíku najdete v přehledových zdrojích, například odkaz.
Hlavní izotopy a jejich charakteristiky
Protium (označované také 1H nebo protium) má jádro tvořené pouze jedním protonem a žádným neutronem. Deuterium (2H nebo deuterium, často zkracováno D) obsahuje jeden proton a jeden neutron; v přírodě se vyskytuje ve stopovém množství. Tritium (3H nebo tritium, T) má dva neutrony a je radioaktivní; jeho přirozený výskyt je velmi malý, většina tritia vzniká uměle nebo kosmickým zářením. Tritium se rozpadá betaem na helium‑3 a má poločas rozpadu přibližně 12 let, proto je označováno jako radioizotop (více o radioaktivitě).
Fyzikální a chemické vlastnosti
Rozdíl v počtu neutronů mění hmotnost jádra, což ovlivňuje fyzikální vlastnosti sloučenin. Například voda obsahující deuterium (D2O, tzv. těžká voda) má jiné hustoty, body varu a tepelné vlastnosti než obyčejná voda. Chemicky jsou izotopy podobné, ale projevuje se izotopový efekt — reakční rychlosti a spektrální čáry se u D nebo T liší od protiu. Deuterium se používá pro spektrální studie (deuterované rozpouštědlo v NMR) i jako indikátor v experimentech, tritium se kromě toho využívá také jako zdroj beta záření a ve studiích stopování.
Historie objevů a výroba
Deuterium byl objeven v roce 1931 a jeho objevení otevřelo novou etapu ve studiu atomových jader a chemických izotopů. Tritium bylo identifikováno a připraveno ve 30. letech 20. století; od té doby se vyrábí i technickými postupy v jaderných reaktorech nebo pomocí urychlovačů částic. Mimo hlavní trojici izolovali vědci v laboratořích i další velmi nestabilní izotopy vodíku (4H až 7H), ale ty se v přírodě nevyskytují a žijí jen zlomek sekundy.
Využití a význam
- Deuterium: výroba těžké vody, analytické metody (NMR, izotopové značení), studií chemických mechanismů.
- Tritium: zdroj beta částic pro osvětlení, stopovací metoda v biologii a ekologii, palivo v experimentech s termojadernou fúzí.
- Protium: základní chemické a biologické procesy — tvoří většinu vodíku ve vesmíru i na Zemi.
- Kosmologie: poměr deuteria k protiu v kosmických objektech slouží jako indikátor podmínek raného vesmíru a hustoty baričí hmoty.
Rozlišení, pojmenování a poznámky
Izotopy vodíku jsou netypické tím, že mají vlastní jména (protium, deuterium, tritium) a pro ně se často používají symboly D a T. Mezinárodní chemické a fyzikální organizace preferují standardní nuklidorové označení 1H, 2H a 3H, ale zvyklosti jmenné terminologie přetrvávají. Další informace o nomenklatuře lze nalézt u odborných institucí (příslušné doporučení).
Pro doplňující čtení a technické detaily jsou dostupné zdroje zaměřené na jadernou fyziku, izotopovou chemii a aplikace v energetice a životním prostředí; vybrané přehledy a databáze lze najít například zde nebo v dalších specializovaných odkazech (protium, deuterium, tritium, radioaktivita, souhrn).