Boyleův zákon (nazývaný také Mariottův zákon nebo Boyle-Mariottův zákon) je zákon o ideálních plynech.
Zákon lze formulovat následovně:
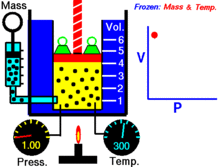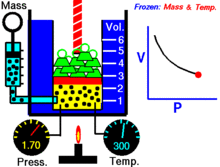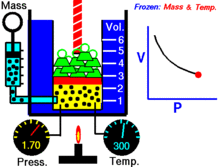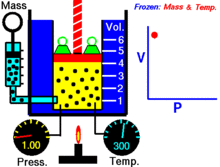
Pro pevné množství ideálního plynu udržovaného při pevné teplotě jsou hodnoty P (tlak) a V (objem) nepřímo úměrné.
Jinými slovy, objem konstantní hmotnosti ideálního plynu při konstantní teplotě je nepřímo úměrný tlaku, který na něj působí.
V symbolech je zákon následující:
P ∝ 1 V {\displaystyle P\propto {\frac {1}{V}}}
nebo
P V = k {\displaystyle PV=k}
kde P je tlak plynu, V je objem plynu a k je konstanta.
Pro danou hmotnost plynu při konstantní teplotě je součin tlaku a objemu konstantní. S klesajícím objemem se úměrně zvyšuje tlak a naopak. Například když se tlak sníží na polovinu, objem se zdvojnásobí.
Předpokládejme, že máte nádrž, která obsahuje určitý objem plynu při určitém tlaku. Když objem nádrže zmenšíte, stejný počet částic plynu se nyní nachází v menším prostoru. Počet srážek se tedy zvýší. Proto je tlak větší.
Představte si, že máte plyn o určitém tlaku (P1) a objemu (V1). Pokud změníte tlak na novou hodnotu (P2), změní se i objem na novou hodnotu (V2). K popisu obou souborů podmínek můžeme použít Boyleův zákon:
P 1 V 1 = k {\displaystyle P_{1}V_{1}=k}
P 2 V 2 = k {\displaystyle P_{2}V_{2}=k}
Konstanta k je v obou případech stejná, takže můžeme říci následující:
P 1 V 1 = P 2 V 2 {\displaystyle P_{1}V_{1}=P_{2}V_{2}}
Příklad: Tlak plynu je 3 atm a jeho objem je 5 litrů. Pokud tlak snížíme na 2 atm, jaký je jeho objem?
P 1 V 1 = P 2 V 2 {\displaystyle P_{1}V_{1}=P_{2}V_{2}}
V 2 = P 1 V 1 P 2 {\displaystyle V_{2}={\frac {P_{1}V_{1}}{P_{2}}}}
V 2 = 3 ∗ 5 2 {\displaystyle V_{2}={\frac {3*5}{2}}}
V 2 = 15 2 {\displaystyle V_{2}={\frac {15}{2}}}
V 2 = 7,5 {\displaystyle V_{2}=7,5}
∴ Objem bude 7,5 litru.
Zákon objevil Robert Boyle v roce 1662 a poté nezávisle na něm Edme Mariotte v roce 1679.