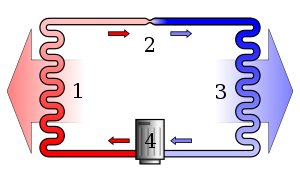
Druhý termodynamický zákon říká, že když se energie mění z jedné formy na jinou nebo se hmota volně pohybuje, entropie (neuspořádanost) v uzavřeném systému se zvyšuje.
Rozdíly v teplotě, tlaku a hustotě se po určité době horizontálně vyrovnají. Vzhledem ke gravitační síle se hustota a tlak ve svislém směru nevyrovnávají. Hustota a tlak na dně budou větší než nahoře.
Entropie je mírou šíření hmoty a energie všude, kam mají přístup.
Nejběžnější formulace druhého termodynamického zákona je v podstatě dílem Rudolfa Clausia:
Jinými slovy, vše se snaží udržet stejnou teplotu po celou dobu.
Existuje mnoho výroků druhého zákona, které používají různé termíny, ale všechny znamenají totéž. Další Clausiův výrok zní:
Teplo samo o sobě nemůže přecházet z chladnějšího tělesa na teplejší.
Obdobný výrok lorda Kelvina zní:
Přeměna, jejímž jediným konečným výsledkem je přeměna tepla získaného ze zdroje při konstantní teplotě na práci, je nemožná.
Druhý zákon platí pouze pro velké systémy. Druhý zákon se týká pravděpodobného chování systému, do kterého se nedostává žádná energie ani hmota. Čím větší je systém, tím pravděpodobněji bude druhý zákon platit.
Otázky a odpovědi
Otázka: Co je druhý termodynamický zákon?
Odpověď: Druhý termodynamický zákon říká, že když se energie mění z jedné formy na druhou nebo se hmota volně pohybuje, entropie (neuspořádanost) v uzavřeném systému se zvyšuje.
Otázka: Co má tendenci se v průběhu času horizontálně vyrovnávat?
Odpověď: Rozdíly v teplotě, tlaku a hustotě mají tendenci se po určité době horizontálně vyrovnávat.
Otázka: Proč se hustota a tlak nevyrovnávají vertikálně?
Odpověď: Kvůli gravitační síle se hustota a tlak nevyrovnávají vertikálně. Hustota a tlak dole budou větší než nahoře.
Otázka: Co je to entropie?
Odpověď: Entropie je míra šíření hmoty a energie všude, kam mají přístup.
Otázka: Jaká je nejčastější formulace druhého termodynamického zákona?
Odpověď: Nejběžnější formulace druhého termodynamického zákona je v podstatě zásluhou Rudolfa Clausia: Vše se snaží udržet stejnou teplotu v čase.
Otázka: Jaký je další Clausiův výrok týkající se druhého termodynamického zákona?
Odpověď: Dalším Clausiovým výrokem je, že teplo nemůže samo o sobě přecházet z chladnějšího tělesa na teplejší.
Otázka: Na jaký druh soustavy se vztahuje druhý termodynamický zákon?
Odpověď: Druhý termodynamický zákon se vztahuje pouze na velké systémy, do kterých se nedostává žádná energie ani hmota. Čím větší je systém, tím spíše bude druhý zákon platit.